Premessa
Nell’ultimo decennio l’orizzonte della terapia ipolipemizzante si è arricchita di formidabili strumenti terapeutici quali ezitimibe, inibitori della proteina PCSK9 (PCSK9i) e acido bempedoico.
Gli studi su queste molecole hanno permesso non solo di dimostrarne l’efficacia, ma hanno fornito importanti informazioni sull’importanza dell’abbassamento delle LDL nella riduzione del rischio cardiovascolare (CV) e costituiscono la base per rivedere anche le modalità di utilizzo delle statine stesse o di associazioni ad oggi disponibili.
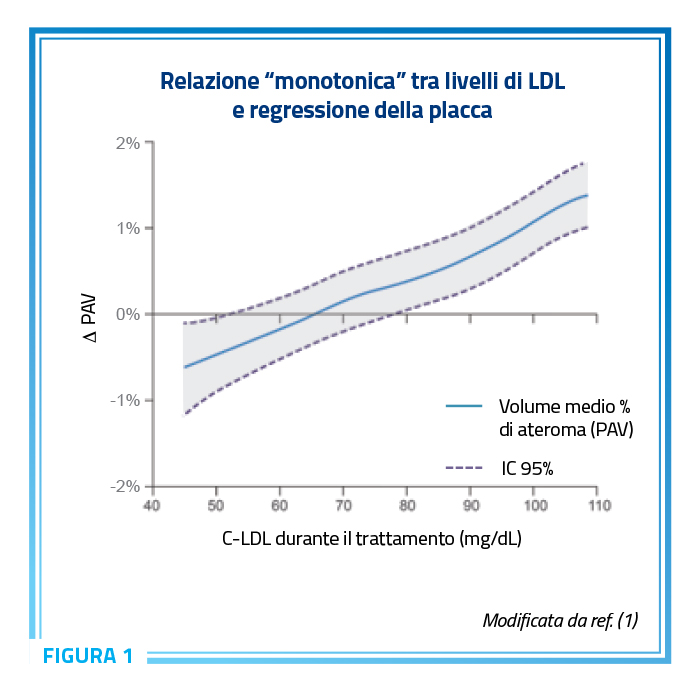
È stata chiaramente dimostrata una relazione “monotonica” tra livelli di LDL, regressione della placca (Figura 1) (1) e rischio cardiovascolare. Nella Figura 1 vediamo come con livelli di LDL via via più bassi si ha una riduzione della progressione della placca aterosclerotica e per livelli inferiori a 65 mg/dl inizia una regressione della placca stessa che è maggiore tanto più le LDL si riducono.
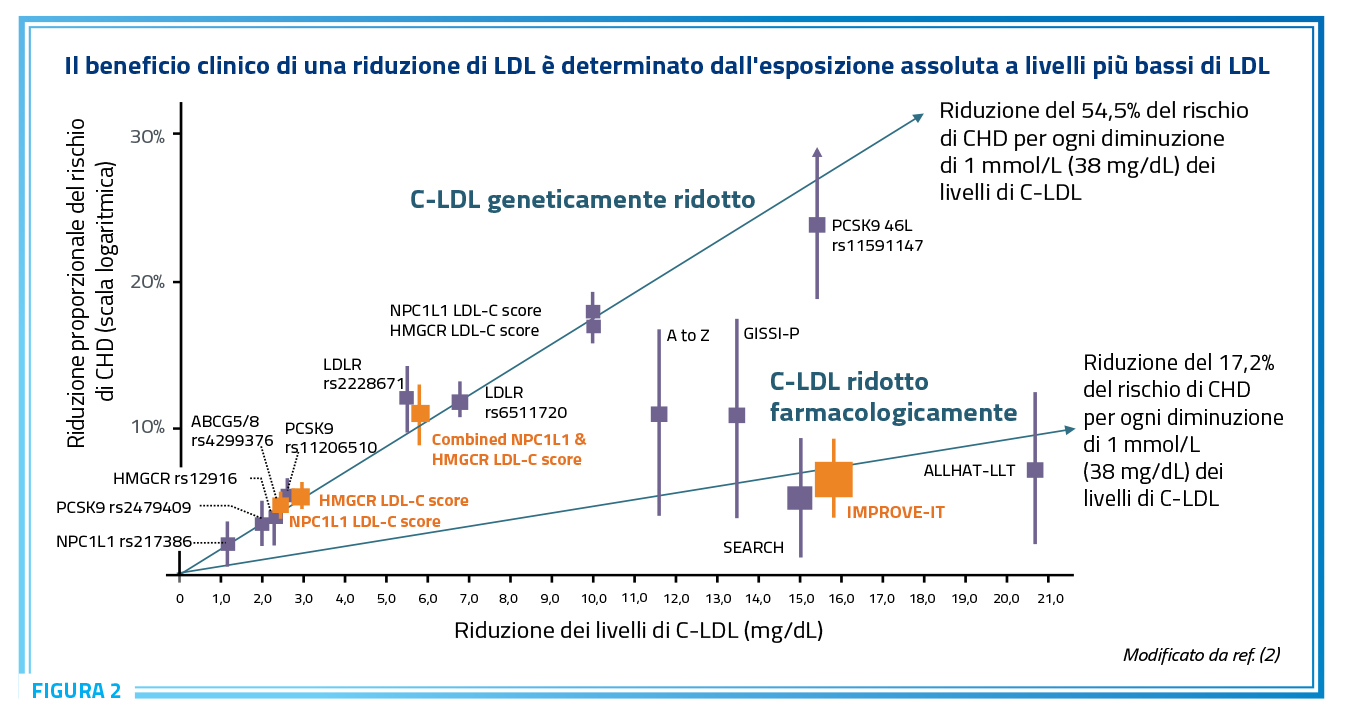
Questo a livello di placca dimostra quello che in modo indiretto si conosceva circa la riduzione del rischio cardiovascolare sia negli studi clinici che negli studi sui pazienti portatori di mutazioni che determinano livelli più bassi di C-LDL (Figura 2) (2).
Nella figura 2 è interessante notare che una riduzione “genetica” dei livelli di LDL determina una riduzione del rischio di decine di volte superiore alla stessa riduzione “farmacologica” ottenuta nei trial, a dimostrazione che ad una precoce riduzione dei valori di C-LDL, corrisponde una importante riduzione del rischio di sviluppo della placca ateromasica. Vedremo in seguito come anche questa osservazione indiretta verrà dimostrata dalle evidenze disponibili.
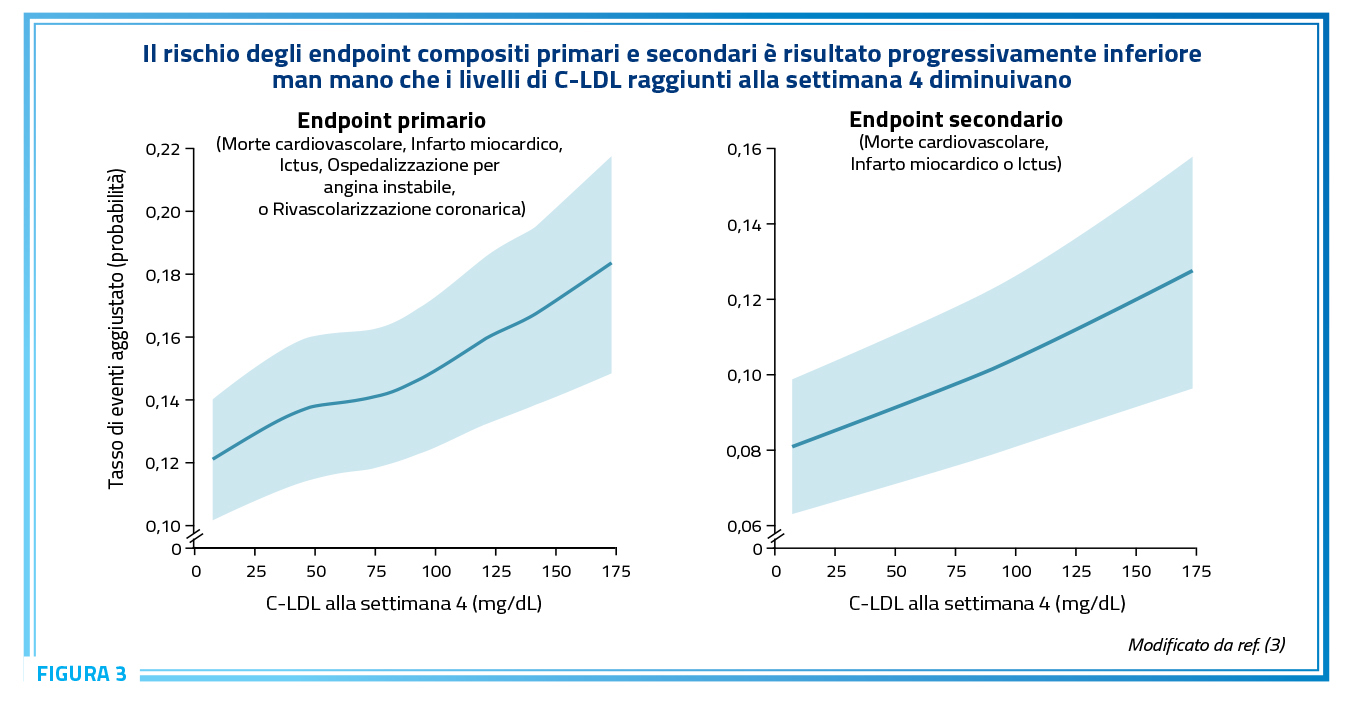
La conferma dei concetti “the lower the better” e “the earlier the better” precedentemente introdotti, deriva anche dai dati dello Studio FOURIER dove con evolocumab i valori di C-LDL si sono abbassati a livello estremo con una relazione anche in questo caso “monotonica” con la riduzione degli eventi CV (Figura 3) (3).
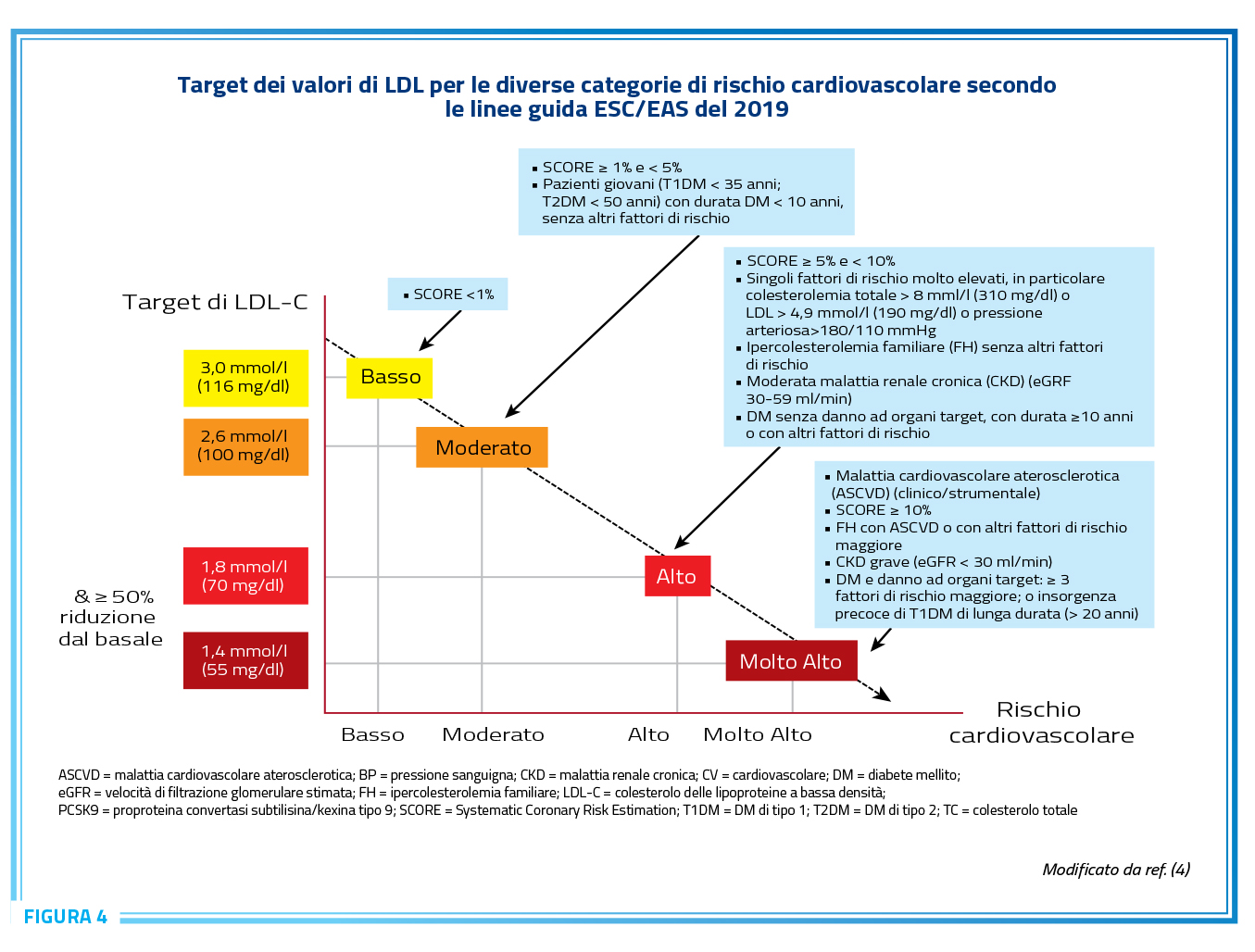
Le linee guida ESC/EAS, ad oggi le più aggiornate, hanno incorporato questi concetti nel 2019 definendo chiaramente il target di C-LDL per le diverse categorie di rischio, rispettivamente < 70mg/dl e 55 mg/dl per le categorie di rischio alto e molto alto (Figura 4) (4).
Al clinico attualmente i problemi che si pongono sono:
1) come raggiungere questi target;
2) come ottenere un’adesione alla terapia, ovvero come massimizzare la aderenza terapeutica.
1) Come raggiungere i target?
Gli studi a partire dagli anni ‘90 hanno definito la potenza terapeutica delle diverse statine nella riduzione dei livelli di colesterolo ed è emerso che le statine più efficaci sono rosuvastatina ed atorvastatina, per questo definite statine a media e alta potenza. Nello stesso modo possiamo dire che per ciascuna statina è ben chiara la riduzione media dei livelli di C-LDL (Figura 5) e che, dato una riduzione di colesterolo, l’effetto di un incremento di dose della statina al livello successivo più alto è del 6% per ogni gradino di aumento di dosaggio (5).
Il principale problema nell’uso delle statine è la scarsa aderenza legata agli effetti collaterali molto fastidiosi per il paziente, come le mialgie e le tendinopatie, e sicuramente per questa classe di farmaci vi è un importante effetto nocebo. Le statine sono tra i farmaci più frequentemente interrotti da parte del paziente e l’interruzione della statina (specie le alte dosi) si associa ad un aumento della mortalità (6). Sebbene vada tenuto presente il rischio di diabete associato alle alte dosi di statine, che in diverse metanalisi si attesta intorno al 9-12%, il beneficio in prevenzione CV rimane imprescindibile e superiore al rischio di sviluppare diabete di nuova insorgenza.
Gli effetti collaterali sono dose dipendente e molecola dipendente e questo va tenuto in conto nella scelta della dose e delle modalità di somministrazione.
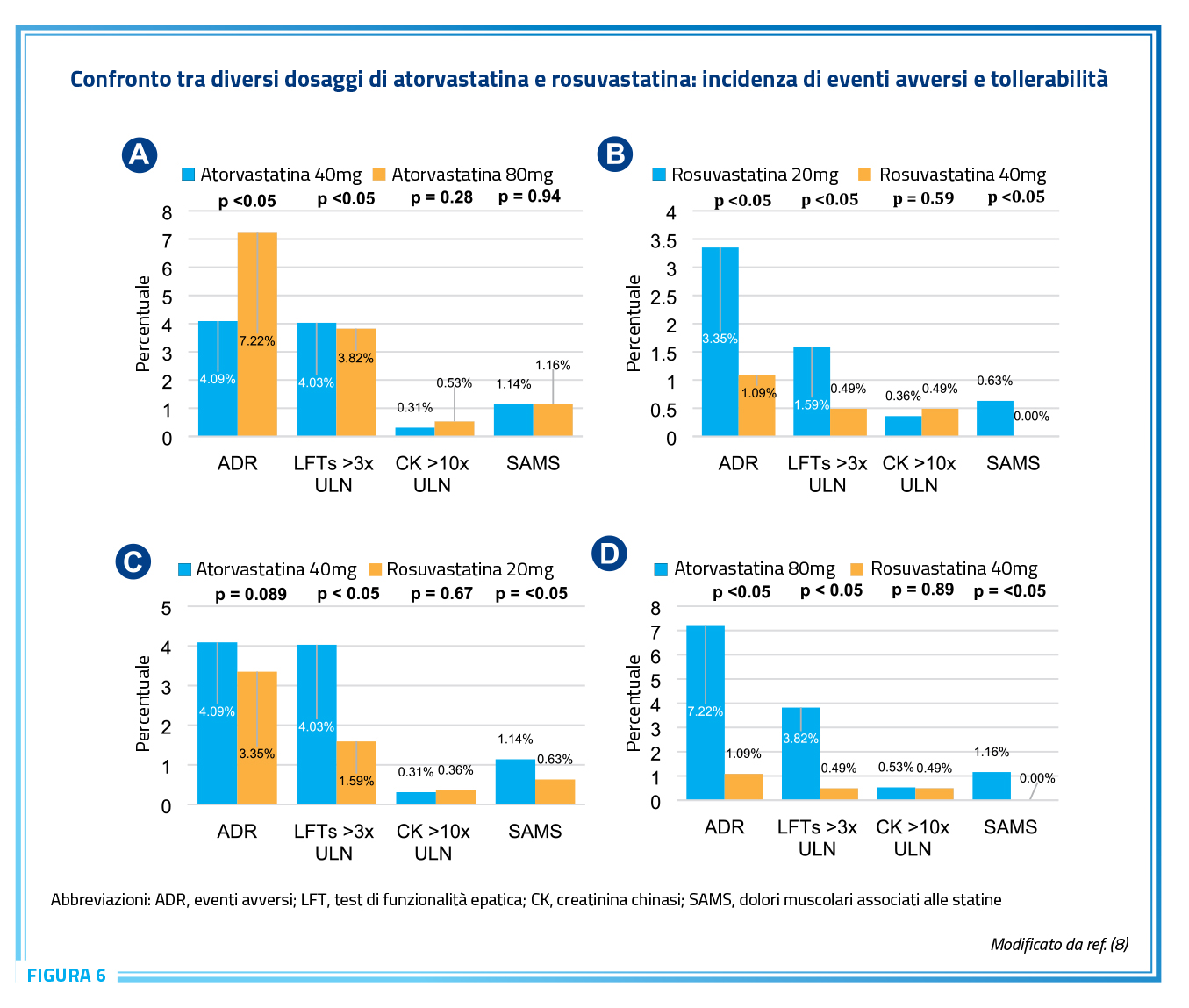
Per quanto riguarda le due statine che costituiscono il “bench mark” (rosuvastatina e atorvastatina), studi di confronto (Figura 6) hanno dimostrato che, sia per le dosi medie che per le alte dosi, rosuvastatina ha effetti collaterali minori in termini di mialgie e movimento markers epatici e che a parità di riduzione dei livelli di C-LDL è possibile utilizzare una dose più bassa di rosuvastatina riducendo quindi ulteriormente la probabilità di effetti collaterali (7).
Arriviamo a questo punto al secondo concetto nella ottimizzazione della terapia ipolipemizzante nelle diverse classi di rischio.
2) Come ottenere un’adesione alla terapia?
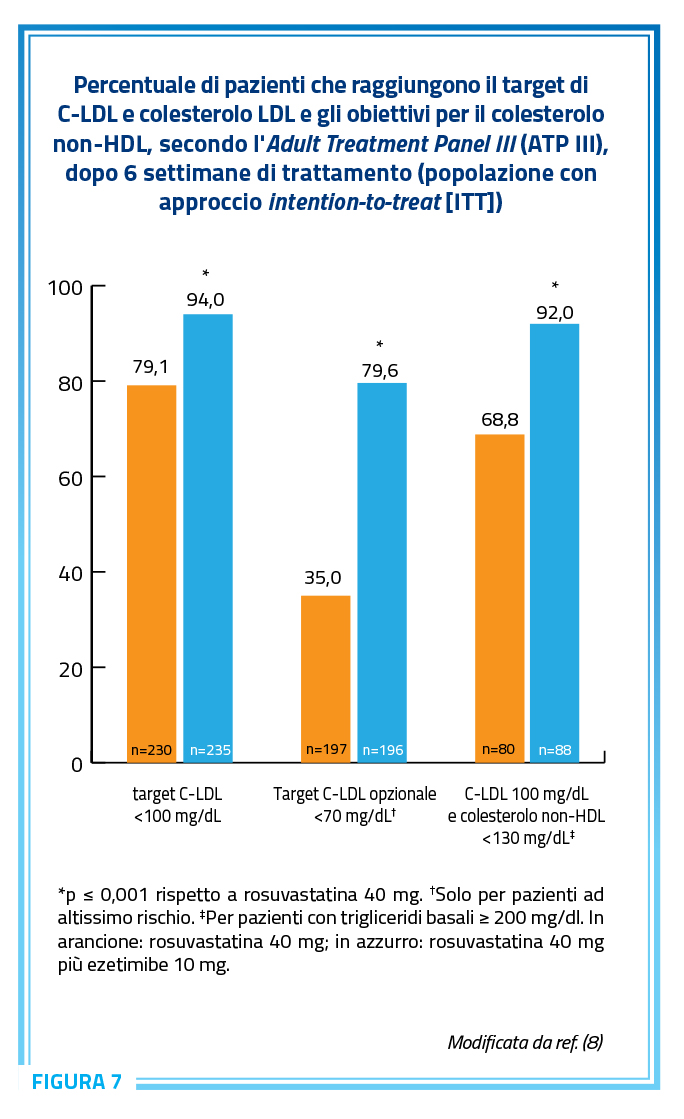
Ezitimibe, limitando l’assorbimento del colesterolo attraverso il blocco del recettore Neiman-Pick C1 riduce in monoterapia i livelli di C-LDL in media del 20%. mentre, L’associazione di ezetimibe con una statina in unica pillola (single pill) consente una riduzione complessiva del C-LDL fino al 50-55% (5). Quando la statina utilizzata è ad alta intensità, i livelli di riduzione possono arrivare in media al 65% (Figura 7), superando l’efficacia di una statina ad alta dose da sola del 5-15%. Meritevoli di menzione, a questo riguardo, i risultati dello studio EXamination of Potential Lipid modifying effects Of Rosuvastatin in combination with Ezetimibe versus Rosuvastatin alone (EXPLORER) condotto in pazienti ipercolestoremici con storia di malattia coronarica, o evidenza clinica di aterosclerosi o un livello di rischio cardiovascolare equivalente alla coronaropatia. La terapia di combinazione rosuvastatina 40 mg + ezetimibe 10 mg ha determinato una riduzione del colesterolo LDL del 69,8% rispetto al basale consentendo il raggiungimento nel 94,0% dei pazienti del target di colesterolo LDL <100 mg/dl e nel 79,6% dei pazienti del target più ambizioso <70 mg/dL (Figura 7) (8). Risultati analoghi sono stati descritti in uno studio di minori dimensioni condotto in pazienti con iperlipidemia severa resistente al trattamento con rosuvastatina nei quali la terapia di combinazione rosuvastatina 40 mg + ezetimibe 10 mg ha determinato una riduzione della colesterolemia LDL del 51% consentendo a circa la metà dei pazienti di raggiungere un target di colesterolo LDL <100 mg/dL (9). Questi risultati dimostrano come la combinazione rosuvastatina 40 mg + ezetimibe 10 mg possa rappresentare uno strumento terapeutico particolarmente efficace in quei pazienti che, in ragione di un profilo di rischio estremamente elevato, necessitano di importanti riduzioni della colesterolemia.
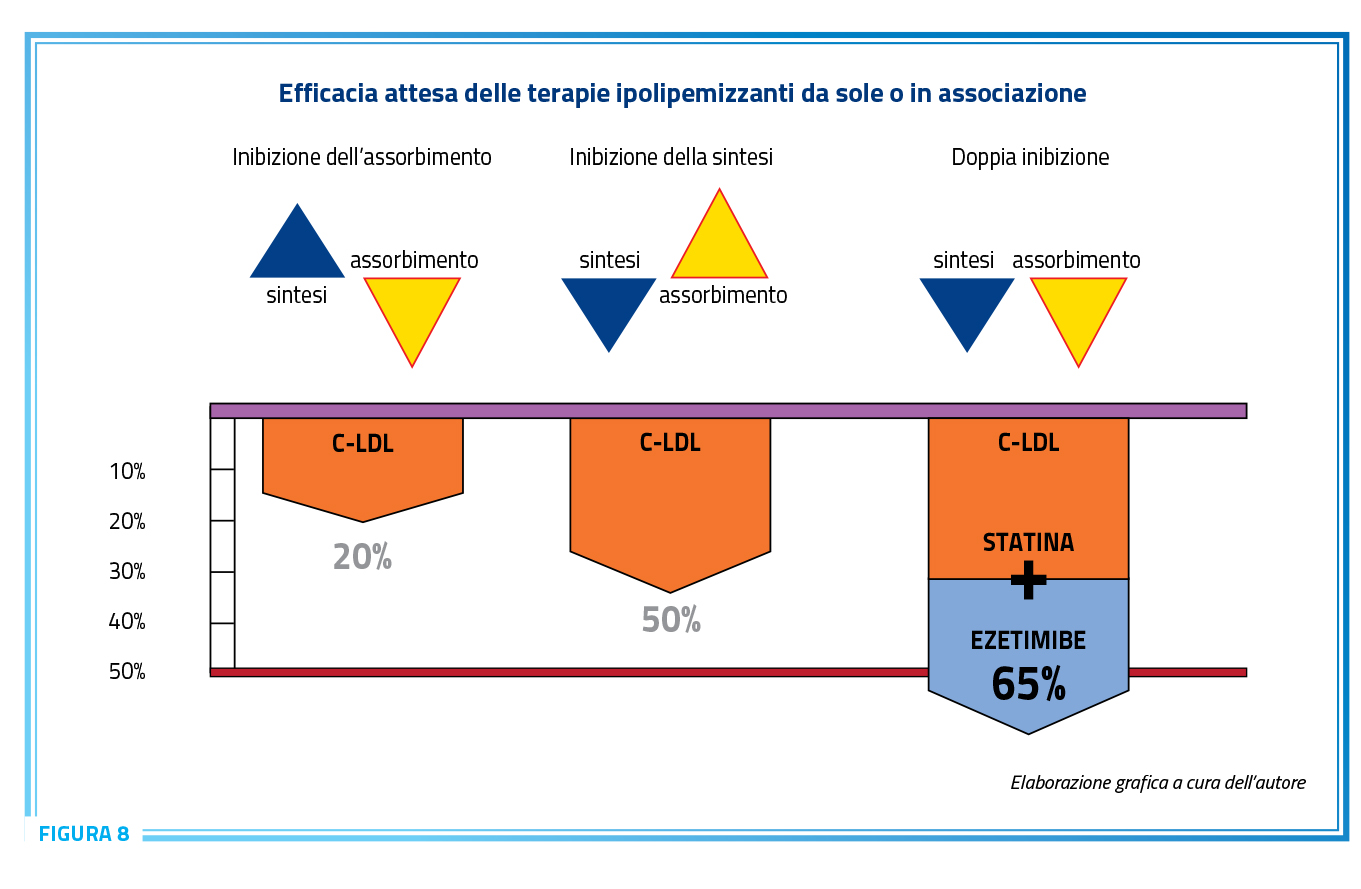
La sinergia statina/ezetimibe è resa possibile dai meccanismi d’azione complementari dei due farmaci: la statina agisce sulla sintesi epatica del colesterolo, mentre ezetimibe interviene sul suo assorbimento intestinale. L’effetto combinato consente di ottenere una riduzione dei livelli di C-LDL in modo omogeneo e prevedibile tra i pazienti, semplificando il compito del medico prescrittore nel raggiungimento degli obiettivi terapeutici (10) (Figura 8).
Questo concetto è molto importante per ottenere l’aderenza terapeutica. È noto che una scarsa aderenza terapeutica si associa ad aumentati eventi cardiovascolari e la sospensione della statina aumenta la mortalità (11).
Recenti registri internazionali hanno dimostrato che il raggiungimento dell’obbiettivo terapeutico di C-LDL a target è in circa il 50% dei pazienti e i principali motivi di non raggiungimento del target sono la percezione di effetti collaterali, il mancato controllo da parte del medico di incrementare la dose e il sottouso di associazioni precostituite.
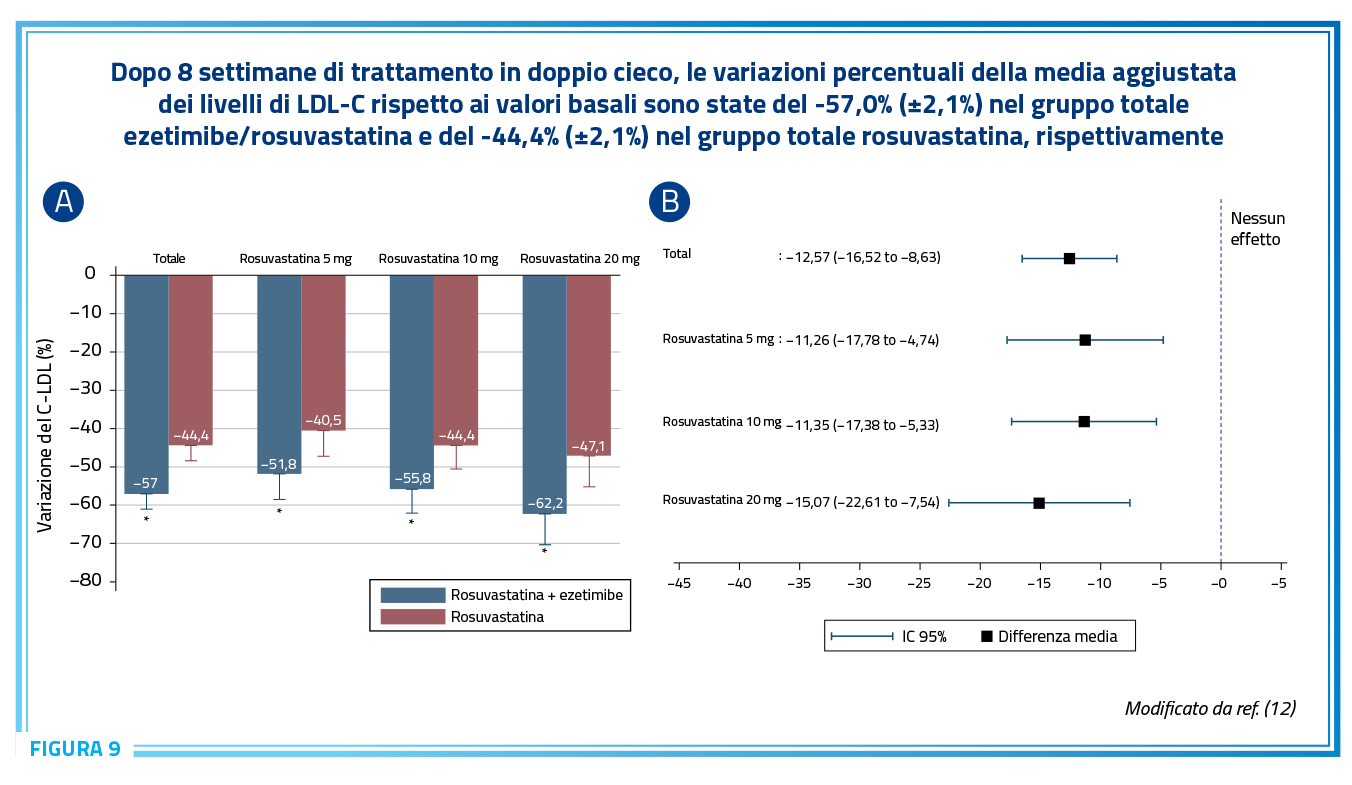
Ecco, quindi, che la gestione clinica del paziente deve partire da una valutazione del rischio del singolo paziente e da un calcolo dei valori ottimali di C-LDL per quella categoria di rischio. A questo punto la scelta della terapia deve focalizzarsi in modo matematico sulla associazione che permette di scegliere una dose più bassa di statina possibile (quindi prevedibilmente più tollerata), ma sempre ottimizzata sulla risposta media che il paziente avrà. In generale la associazione rosuvastatina/ezitimibe è quella più efficiente da questo punto di vista (Figura 9) (12) e si associa ad un aumento del 44% della aderenza terapeutica (13).
Più recentemente, il confronto tra una strategia basata su alte dosi di statine oppure una strategia di associazione statina ed ezitimibe è stata studiata formalmente in modo randomizzato in due trials, lo studio RACING (14) e lo studio LODESTAR (15).
Nello studio RACING, è stato confrontato il trattamento in monoterapia con rosuvastatina 20 mg versus la terapia di associazione costituita da rosuvastatina 10/ ezetimibe 10 in 3.780 pazienti con patologia aterotrombotica, ovvero in prevenzione secondaria. Lo studio LODESTAR, invece, ha studiato in pazienti con patologia coronarica una strategia di incremento del dosaggio variabile per ottenere target di 50-70 mg/dl (treat-to-target) con diverse strategie inclusive di associazione versus uso di alte dosi di statina iniziale in 4.400 pazienti. In entrambi i trial il follow-up era a tre anni. Gli studi hanno entrambi raggiunto l’end-point, che era l’equivalenza, ma in questa sede analizzeremo i dati cumulati.
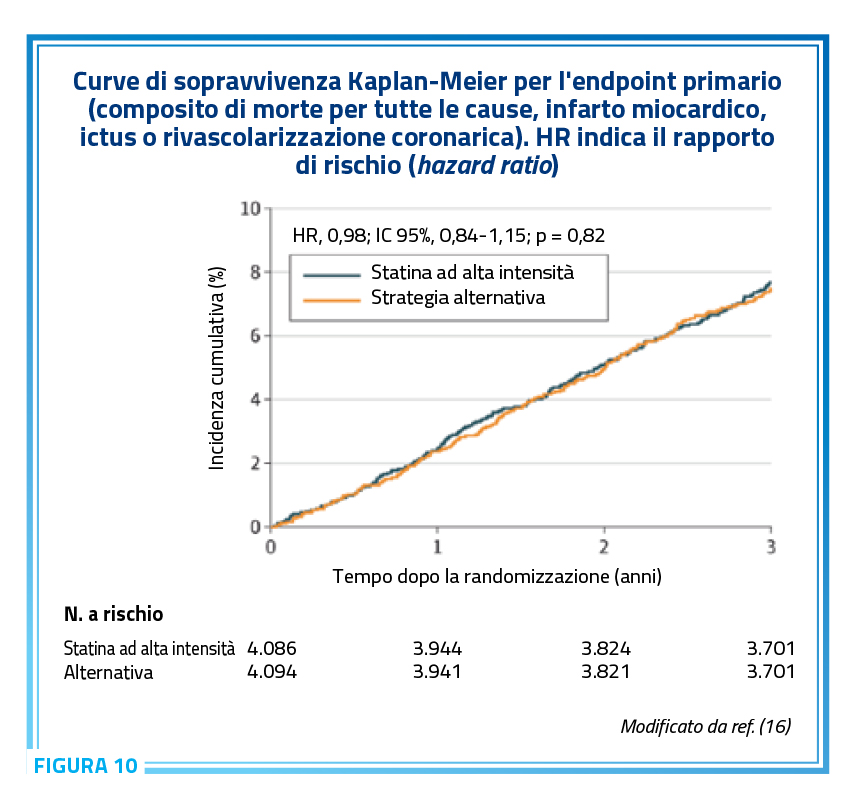
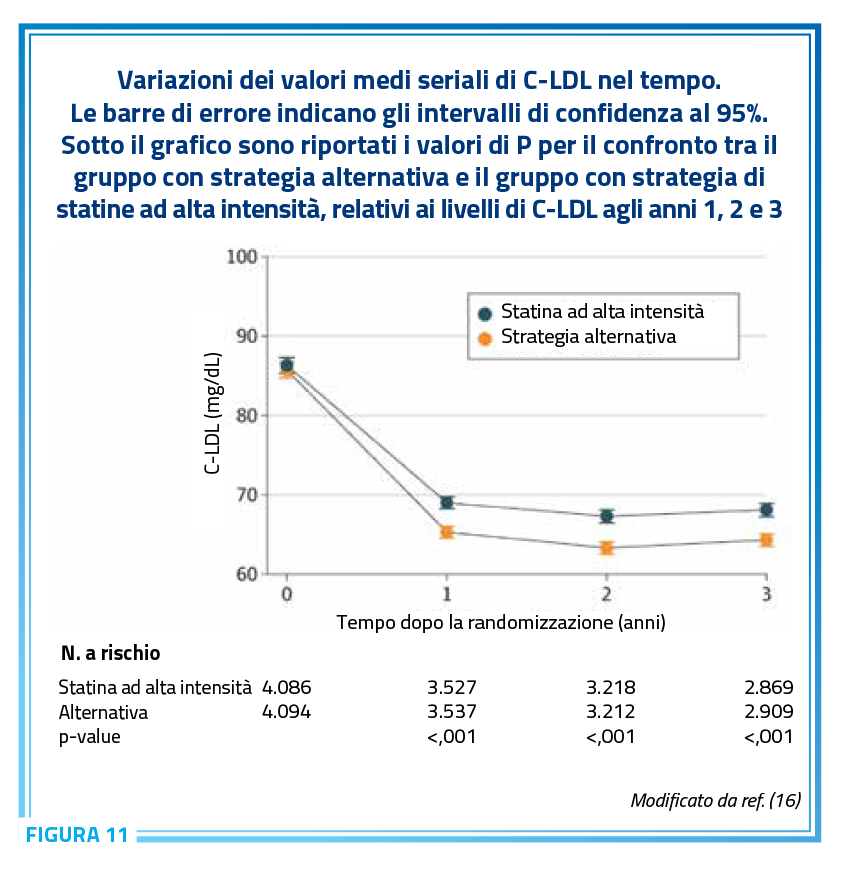
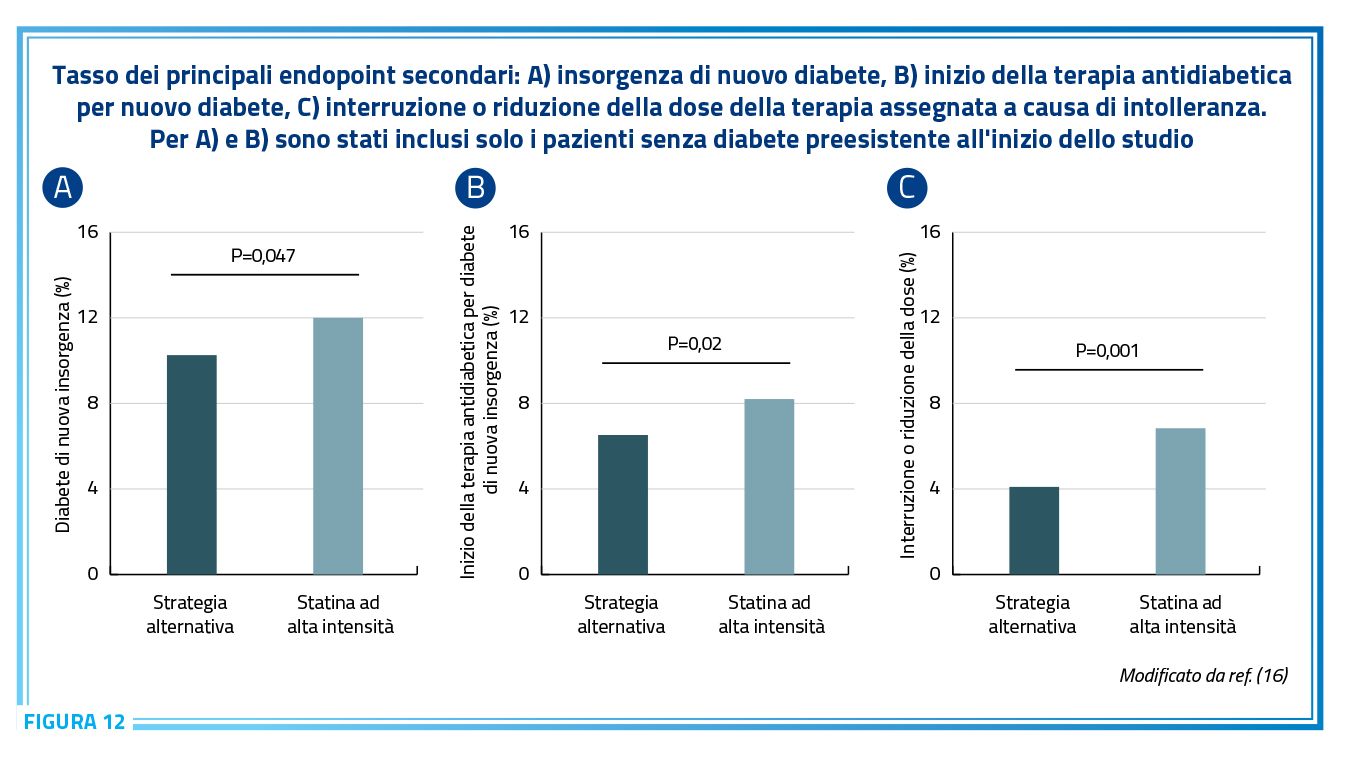
Utilizzando dati individuali dei singoli pazienti di entrambi i trial è stata recentemente pubblicata una metanalisi dei due studi che conferma su un campione di più di 8.000 pazienti come la strategia di associazione (“Strategia alternativa”) è altrettanto efficacie (Figura 10,11) (16) e si associa ad una riduzione significativa della intolleranza (ridotta del 42%) e del rischio di diabete legato alla alta dose di statina (Figura 12) (16).
Conclusioni
In conclusione, se possiamo suggerire il trattamento della dislipidemia nel paziente a rischio cardiovascolare:
- Deve tendere al raggiungimento degli obiettivi terapeutici previsti in rapporto al profilo di rischio del singolo paziente.
- Il target è nei pazienti a rischio moderato il C-LDL < 100 mg/dl, nei pazienti ad alto rischio < 70 mg/dl, infine, nei pazienti a rischio molto alto < 55 mg/dl e se estremo (eventi ricorrenti, multivaso) < 40 mg/dl.
- Deve proseguire indefinitamente e quindi deve essere accettata dal paziente.
- Deve essere prestata particolare attenzione all’aderenza del paziente al trattamento prescritto. Anche se il paziente ha effetto nocebo ne dobbiamo tenere contro perché verosimilmente sospenderà il trattamento.
- La scelta di una strategia con il migliore rapporto rischio/beneficio riduce la probabilità di interruzione del trattamento.
- La terapia di combinazione con ezetimibe + statine è più efficace nella riduzione dei livelli di C-LDL rispetto alla terapia ad alta intensità.
- In caso di mancato target con la associazione anche alla dose più alta va associato PCSK9i che riduce i valori del 50% in aggiunta alle statine. L’acido bempedoico in questo contesto ha un valore incrementale limitato intorno al 9%.
- Le combinazioni statine + altri farmaci (fibrati, niacina, Omega 3) non sono supportate da sufficienti evidenze per raccomandarne l’uso.
Bibliografia
- Nicholls SJ, Tuzcu EM, Sipahi I, Grasso AW, Schoenhagen P, Hu T, et al. Statins, High-Density Lipoprotein Cholesterol, and Regression of Coronary Atherosclerosis. JAMA. 2007 Feb 7;297(5):499.
- Ference BA, Majeed F, Penumetcha R, Flack JM, Brook RD. Effect of Naturally Random Allocation to Lower Low-Density Lipoprotein Cholesterol on the Risk of Coronary Heart Disease Mediated by Polymorphisms in NPC1L1, HMGCR, or Both. J Am Coll Cardiol. 2015 Apr;65(15):1552–61.
- Giugliano RP, Pedersen TR, Park JG, De Ferrari GM, Gaciong ZA, Ceska R, et al. Clinical efficacy and safety of achieving very low LDL-cholesterol concentrations with the PCSK9 inhibitor evolocumab: a prespecified secondary analysis of the FOURIER trial. The Lancet. 2017 Oct;390(10106):1962–71.
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111–88.
- STEIN E. Results of phase I/II clinical trials with ezetimibe, a novel selective cholesterol absorption inhibitor. European Heart Journal Supplements. 2001 Jun;3:E11–6.
- Ho PM, Spertus JA, Masoudi FA, Reid KJ, Peterson ED, Magid DJ, et al. Impact of Medication Therapy Discontinuation on Mortality After Myocardial Infarction. Arch Intern Med. 2006 Sep 25;166(17):1842.
- Stein B, Ward T, Hale G, Lyver E. Safety of High-Intensity Statins in the Veteran Population: Atorvastatin 40 to 80 mg Compared With Rosuvastatin 20 to 40 mg. Annals of Pharmacotherapy. 2020 May 12;54(5):405–13.
- Ballantyne CM, Weiss R, Moccetti T, et al. Efficacy and Safety of Rosuvastatin 40 mg Alone or in Combination WithEzetimibe in Patients at High Risk of Cardiovascular Disease (Results from the EXPLORER Study). Am J Cardiol 2007;99:673-680.
- Leibovitz E, Gavish D, Bitzur R, et al. 2006. Efficacy and safety of rosuvastatin-ezetimibe combination for the treatment of severe hypercholesterolemia [abstract]. Atheroscler Suppl, 7:554 (abstract).
- Poli A. L’associazione ROSUVASTATINA-EZETIMIBE: effetto farmacodinamico sinergico nel trattamento dell’ipercolesterolemia. Quaderni di Medicina e Chirurgia 2020, n. 2, Supplemento n. 1, 2020.
- Volpe M, Degli Esposti L, Romeo F, Trimarco B, Bovenzi FM, Mastromarino V, et al. [Role of adherence to long-term drug therapy in patients with cardiovascular disease: an Italian intersocietary consensus document]. G Ital Cardiol (Rome). 2014 Oct;15(10 Suppl 1):3S-10S.
- Hong SJ, Jeong HS, Ahn JC, Cha DH, Won KH, Kim W, et al. A Phase III, Multicenter, Randomized, Double-blind, Active Comparator Clinical Trial to Compare the Efficacy and Safety of Combination Therapy With Ezetimibe and Rosuvastatin Versus Rosuvastatin Monotherapy in Patients With Hypercholesterolemia: I-ROSETTE (Ildong Rosuvastatin & Ezetimibe for Hypercholesterolemia) Randomized Controlled Trial. Clin Ther [Internet]. 2018 Feb 1;40(2):226-241.e4. Available from: https://doi.org/10.1016/j.clinthera.2017.12.018
- 13. Castellano JM, Sanz G, Fernandez Ortiz A, Garrido E, Bansilal S, Fuster V. A Polypill Strategy to Improve Global Secondary Cardiovascular Prevention. J Am Coll Cardiol. 2014 Aug;64(6):613–21.
- Kim BK, Hong SJ, Lee YJ, Hong SJ, Yun KH, Hong BK, et al. Long-term efficacy and safety of moderate-intensity statin with ezetimibe combination therapy versus high-intensity statin monotherapy in patients with atherosclerotic cardiovascular disease (RACING): a randomised, open-label, non-inferiority trial. The Lancet. 2022 Jul;400(10349):380–90.
- Hong SJ, Lee YJ, Lee SJ, Hong BK, Kang WC, Lee JY, et al. Treat-to-Target or High-Intensity Statin in Patients With Coronary Artery Disease. JAMA. 2023 Apr 4;329(13):1078.
- Lee YJ, Hong BK, Yun KH, Kang WC, Hong SJ, Lee SH, et al. Alternative LDL Cholesterol–Lowering Strategy vs High-Intensity Statins in Atherosclerotic Cardiovascular Disease. JAMA Cardiol. 2024 Nov 20:e243911.
Premessa
Nell’ultimo decennio l’orizzonte della terapia ipolipemizzante si è arricchita di formidabili strumenti terapeutici quali ezitimibe, inibitori della proteina PCSK9 (PCSK9i) e acido bempedoico.
Gli studi su queste molecole hanno permesso non solo di dimostrarne l’efficacia, ma hanno fornito importanti informazioni sull’importanza dell’abbassamento delle LDL nella riduzione del rischio cardiovascolare (CV) e costituiscono la base per rivedere anche le modalità di utilizzo delle statine stesse o di associazioni ad oggi disponibili.
È stata chiaramente dimostrata una relazione “monotonica” tra livelli di LDL, regressione della placca (Figura 1) (1) e rischio cardiovascolare. Nella Figura 1 vediamo come con livelli di LDL via via più bassi si ha una riduzione della progressione della placca aterosclerotica e per livelli inferiori a 65 mg/dl inizia una regressione della placca stessa che è maggiore tanto più le LDL si riducono.
Questo a livello di placca dimostra quello che in modo indiretto si conosceva circa la riduzione del rischio cardiovascolare sia negli studi clinici che negli studi sui pazienti portatori di mutazioni che determinano livelli più bassi di C-LDL (Figura 2) (2).
Nella figura 2 è interessante notare che una riduzione “genetica” dei livelli di LDL determina una riduzione del rischio di decine di volte superiore alla stessa riduzione “farmacologica” ottenuta nei trial, a dimostrazione che ad una precoce riduzione dei valori di C-LDL, corrisponde una importante riduzione del rischio di sviluppo della placca ateromasica. Vedremo in seguito come anche questa osservazione indiretta verrà dimostrata dalle evidenze disponibili.
La conferma dei concetti “the lower the better” e “the earlier the better” precedentemente introdotti, deriva anche dai dati dello Studio FOURIER dove con evolocumab i valori di C-LDL si sono abbassati a livello estremo con una relazione anche in questo caso “monotonica” con la riduzione degli eventi CV (Figura 3) (3).
Le linee guida ESC/EAS, ad oggi le più aggiornate, hanno incorporato questi concetti nel 2019 definendo chiaramente il target di C-LDL per le diverse categorie di rischio, rispettivamente < 70mg/dl e 55 mg/dl per le categorie di rischio alto e molto alto (Figura 4) (4).
Al clinico attualmente i problemi che si pongono sono:
1) come raggiungere questi target;
2) come ottenere un’adesione alla terapia, ovvero come massimizzare la aderenza terapeutica.
1) Come raggiungere i target?
Gli studi a partire dagli anni ‘90 hanno definito la potenza terapeutica delle diverse statine nella riduzione dei livelli di colesterolo ed è emerso che le statine più efficaci sono rosuvastatina ed atorvastatina, per questo definite statine a media e alta potenza. Nello stesso modo possiamo dire che per ciascuna statina è ben chiara la riduzione media dei livelli di C-LDL (Figura 5) e che, dato una riduzione di colesterolo, l’effetto di un incremento di dose della statina al livello successivo più alto è del 6% per ogni gradino di aumento di dosaggio (5).
Il principale problema nell’uso delle statine è la scarsa aderenza legata agli effetti collaterali molto fastidiosi per il paziente, come le mialgie e le tendinopatie, e sicuramente per questa classe di farmaci vi è un importante effetto nocebo. Le statine sono tra i farmaci più frequentemente interrotti da parte del paziente e l’interruzione della statina (specie le alte dosi) si associa ad un aumento della mortalità (6). Sebbene vada tenuto presente il rischio di diabete associato alle alte dosi di statine, che in diverse metanalisi si attesta intorno al 9-12%, il beneficio in prevenzione CV rimane imprescindibile e superiore al rischio di sviluppare diabete di nuova insorgenza.
Gli effetti collaterali sono dose dipendente e molecola dipendente e questo va tenuto in conto nella scelta della dose e delle modalità di somministrazione.
Per quanto riguarda le due statine che costituiscono il “bench mark” (rosuvastatina e atorvastatina), studi di confronto (Figura 6) hanno dimostrato che, sia per le dosi medie che per le alte dosi, rosuvastatina ha effetti collaterali minori in termini di mialgie e movimento markers epatici e che a parità di riduzione dei livelli di C-LDL è possibile utilizzare una dose più bassa di rosuvastatina riducendo quindi ulteriormente la probabilità di effetti collaterali (7).
Arriviamo a questo punto al secondo concetto nella ottimizzazione della terapia ipolipemizzante nelle diverse classi di rischio.
2) Come ottenere un’adesione alla terapia?
Ezitimibe, limitando l’assorbimento del colesterolo attraverso il blocco del recettore Neiman-Pick C1 riduce in monoterapia i livelli di C-LDL in media del 20%. mentre, L’associazione di ezetimibe con una statina in unica pillola (single pill) consente una riduzione complessiva del C-LDL fino al 50-55% (5). Quando la statina utilizzata è ad alta intensità, i livelli di riduzione possono arrivare in media al 65% (Figura 7), superando l’efficacia di una statina ad alta dose da sola del 5-15%. Meritevoli di menzione, a questo riguardo, i risultati dello studio EXamination of Potential Lipid modifying effects Of Rosuvastatin in combination with Ezetimibe versus Rosuvastatin alone (EXPLORER) condotto in pazienti ipercolestoremici con storia di malattia coronarica, o evidenza clinica di aterosclerosi o un livello di rischio cardiovascolare equivalente alla coronaropatia. La terapia di combinazione rosuvastatina 40 mg + ezetimibe 10 mg ha determinato una riduzione del colesterolo LDL del 69,8% rispetto al basale consentendo il raggiungimento nel 94,0% dei pazienti del target di colesterolo LDL <100 mg/dl e nel 79,6% dei pazienti del target più ambizioso <70 mg/dL (Figura 7) (8). Risultati analoghi sono stati descritti in uno studio di minori dimensioni condotto in pazienti con iperlipidemia severa resistente al trattamento con rosuvastatina nei quali la terapia di combinazione rosuvastatina 40 mg + ezetimibe 10 mg ha determinato una riduzione della colesterolemia LDL del 51% consentendo a circa la metà dei pazienti di raggiungere un target di colesterolo LDL <100 mg/dL (9). Questi risultati dimostrano come la combinazione rosuvastatina 40 mg + ezetimibe 10 mg possa rappresentare uno strumento terapeutico particolarmente efficace in quei pazienti che, in ragione di un profilo di rischio estremamente elevato, necessitano di importanti riduzioni della colesterolemia.
La sinergia statina/ezetimibe è resa possibile dai meccanismi d’azione complementari dei due farmaci: la statina agisce sulla sintesi epatica del colesterolo, mentre ezetimibe interviene sul suo assorbimento intestinale. L’effetto combinato consente di ottenere una riduzione dei livelli di C-LDL in modo omogeneo e prevedibile tra i pazienti, semplificando il compito del medico prescrittore nel raggiungimento degli obiettivi terapeutici (10) (Figura 8).
Questo concetto è molto importante per ottenere l’aderenza terapeutica. È noto che una scarsa aderenza terapeutica si associa ad aumentati eventi cardiovascolari e la sospensione della statina aumenta la mortalità (11).
Recenti registri internazionali hanno dimostrato che il raggiungimento dell’obbiettivo terapeutico di C-LDL a target è in circa il 50% dei pazienti e i principali motivi di non raggiungimento del target sono la percezione di effetti collaterali, il mancato controllo da parte del medico di incrementare la dose e il sottouso di associazioni precostituite.
Ecco, quindi, che la gestione clinica del paziente deve partire da una valutazione del rischio del singolo paziente e da un calcolo dei valori ottimali di C-LDL per quella categoria di rischio. A questo punto la scelta della terapia deve focalizzarsi in modo matematico sulla associazione che permette di scegliere una dose più bassa di statina possibile (quindi prevedibilmente più tollerata), ma sempre ottimizzata sulla risposta media che il paziente avrà. In generale la associazione rosuvastatina/ezitimibe è quella più efficiente da questo punto di vista (Figura 9) (12) e si associa ad un aumento del 44% della aderenza terapeutica (13).
Più recentemente, il confronto tra una strategia basata su alte dosi di statine oppure una strategia di associazione statina ed ezitimibe è stata studiata formalmente in modo randomizzato in due trials, lo studio RACING (14) e lo studio LODESTAR (15).
Nello studio RACING, è stato confrontato il trattamento in monoterapia con rosuvastatina 20 mg versus la terapia di associazione costituita da rosuvastatina 10/ ezetimibe 10 in 3.780 pazienti con patologia aterotrombotica, ovvero in prevenzione secondaria. Lo studio LODESTAR, invece, ha studiato in pazienti con patologia coronarica una strategia di incremento del dosaggio variabile per ottenere target di 50-70 mg/dl (treat-to-target) con diverse strategie inclusive di associazione versus uso di alte dosi di statina iniziale in 4.400 pazienti. In entrambi i trial il follow-up era a tre anni. Gli studi hanno entrambi raggiunto l’end-point, che era l’equivalenza, ma in questa sede analizzeremo i dati cumulati.
Utilizzando dati individuali dei singoli pazienti di entrambi i trial è stata recentemente pubblicata una metanalisi dei due studi che conferma su un campione di più di 8.000 pazienti come la strategia di associazione (“Strategia alternativa”) è altrettanto efficacie (Figura 10,11) (16) e si associa ad una riduzione significativa della intolleranza (ridotta del 42%) e del rischio di diabete legato alla alta dose di statina (Figura 12) (16).
Conclusioni
In conclusione, se possiamo suggerire il trattamento della dislipidemia nel paziente a rischio cardiovascolare:
- Deve tendere al raggiungimento degli obiettivi terapeutici previsti in rapporto al profilo di rischio del singolo paziente.
- Il target è nei pazienti a rischio moderato il C-LDL < 100 mg/dl, nei pazienti ad alto rischio < 70 mg/dl, infine, nei pazienti a rischio molto alto < 55 mg/dl e se estremo (eventi ricorrenti, multivaso) < 40 mg/dl.
- Deve proseguire indefinitamente e quindi deve essere accettata dal paziente.
- Deve essere prestata particolare attenzione all’aderenza del paziente al trattamento prescritto. Anche se il paziente ha effetto nocebo ne dobbiamo tenere contro perché verosimilmente sospenderà il trattamento.
- La scelta di una strategia con il migliore rapporto rischio/beneficio riduce la probabilità di interruzione del trattamento.
- La terapia di combinazione con ezetimibe + statine è più efficace nella riduzione dei livelli di C-LDL rispetto alla terapia ad alta intensità.
- In caso di mancato target con la associazione anche alla dose più alta va associato PCSK9i che riduce i valori del 50% in aggiunta alle statine. L’acido bempedoico in questo contesto ha un valore incrementale limitato intorno al 9%.
- Le combinazioni statine + altri farmaci (fibrati, niacina, Omega 3) non sono supportate da sufficienti evidenze per raccomandarne l’uso.
Bibliografia
- Nicholls SJ, Tuzcu EM, Sipahi I, Grasso AW, Schoenhagen P, Hu T, et al. Statins, High-Density Lipoprotein Cholesterol, and Regression of Coronary Atherosclerosis. JAMA. 2007 Feb 7;297(5):499.
- Ference BA, Majeed F, Penumetcha R, Flack JM, Brook RD. Effect of Naturally Random Allocation to Lower Low-Density Lipoprotein Cholesterol on the Risk of Coronary Heart Disease Mediated by Polymorphisms in NPC1L1, HMGCR, or Both. J Am Coll Cardiol. 2015 Apr;65(15):1552–61.
- Giugliano RP, Pedersen TR, Park JG, De Ferrari GM, Gaciong ZA, Ceska R, et al. Clinical efficacy and safety of achieving very low LDL-cholesterol concentrations with the PCSK9 inhibitor evolocumab: a prespecified secondary analysis of the FOURIER trial. The Lancet. 2017 Oct;390(10106):1962–71.
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111–88.
- STEIN E. Results of phase I/II clinical trials with ezetimibe, a novel selective cholesterol absorption inhibitor. European Heart Journal Supplements. 2001 Jun;3:E11–6.
- Ho PM, Spertus JA, Masoudi FA, Reid KJ, Peterson ED, Magid DJ, et al. Impact of Medication Therapy Discontinuation on Mortality After Myocardial Infarction. Arch Intern Med. 2006 Sep 25;166(17):1842.
- Stein B, Ward T, Hale G, Lyver E. Safety of High-Intensity Statins in the Veteran Population: Atorvastatin 40 to 80 mg Compared With Rosuvastatin 20 to 40 mg. Annals of Pharmacotherapy. 2020 May 12;54(5):405–13.
- Ballantyne CM, Weiss R, Moccetti T, et al. Efficacy and Safety of Rosuvastatin 40 mg Alone or in Combination WithEzetimibe in Patients at High Risk of Cardiovascular Disease (Results from the EXPLORER Study). Am J Cardiol 2007;99:673-680.
- Leibovitz E, Gavish D, Bitzur R, et al. 2006. Efficacy and safety of rosuvastatin-ezetimibe combination for the treatment of severe hypercholesterolemia [abstract]. Atheroscler Suppl, 7:554 (abstract).
- Poli A. L’associazione ROSUVASTATINA-EZETIMIBE: effetto farmacodinamico sinergico nel trattamento dell’ipercolesterolemia. Quaderni di Medicina e Chirurgia 2020, n. 2, Supplemento n. 1, 2020.
- Volpe M, Degli Esposti L, Romeo F, Trimarco B, Bovenzi FM, Mastromarino V, et al. [Role of adherence to long-term drug therapy in patients with cardiovascular disease: an Italian intersocietary consensus document]. G Ital Cardiol (Rome). 2014 Oct;15(10 Suppl 1):3S-10S.
- Hong SJ, Jeong HS, Ahn JC, Cha DH, Won KH, Kim W, et al. A Phase III, Multicenter, Randomized, Double-blind, Active Comparator Clinical Trial to Compare the Efficacy and Safety of Combination Therapy With Ezetimibe and Rosuvastatin Versus Rosuvastatin Monotherapy in Patients With Hypercholesterolemia: I-ROSETTE (Ildong Rosuvastatin & Ezetimibe for Hypercholesterolemia) Randomized Controlled Trial. Clin Ther [Internet]. 2018 Feb 1;40(2):226-241.e4. Available from: https://doi.org/10.1016/j.clinthera.2017.12.018
- 13. Castellano JM, Sanz G, Fernandez Ortiz A, Garrido E, Bansilal S, Fuster V. A Polypill Strategy to Improve Global Secondary Cardiovascular Prevention. J Am Coll Cardiol. 2014 Aug;64(6):613–21.
- Kim BK, Hong SJ, Lee YJ, Hong SJ, Yun KH, Hong BK, et al. Long-term efficacy and safety of moderate-intensity statin with ezetimibe combination therapy versus high-intensity statin monotherapy in patients with atherosclerotic cardiovascular disease (RACING): a randomised, open-label, non-inferiority trial. The Lancet. 2022 Jul;400(10349):380–90.
- Hong SJ, Lee YJ, Lee SJ, Hong BK, Kang WC, Lee JY, et al. Treat-to-Target or High-Intensity Statin in Patients With Coronary Artery Disease. JAMA. 2023 Apr 4;329(13):1078.
- Lee YJ, Hong BK, Yun KH, Kang WC, Hong SJ, Lee SH, et al. Alternative LDL Cholesterol–Lowering Strategy vs High-Intensity Statins in Atherosclerotic Cardiovascular Disease. JAMA Cardiol. 2024 Nov 20:e243911.
Related papers
Lo scenario della medicina attuale è caratterizzato da elementi di complessità generale inimmaginabili due decenni fa ed in grado di rendere molto più difficile la pratica clinica giornaliera. In particolare, la coesistenza di multiple condizioni passibili di un trattamento farmacologico nello stesso soggetto condiziona in maniera forzata alcune delle scelte terapeutiche spingendo alla ricerca di [more info]
Colesterolemia subottimale come fattore di rischio per le malattie cardiovascolari Il miglioramento delle abitudini alimentari e l’ottimizzazione dei livelli di colesterolo LDL nel sangue – fattore causale e cumulativo - sembrano essere strumenti efficaci per ridurre il rischio di malattie cardiovascolari su base aterosclerotica, che ancora oggi rappresentano una delle principali cause di morte e [more info]
Introduzione Le malattie cardiovascolari (CV) rappresentano la principale causa di morbilità e mortalità a livello mondiale (1). Sebbene le tecnologie mediche e i trattamenti farmacologici abbiano raggiunto livelli di avanguardia, il Sistema Sanitario globale si trova a fronteggiare un crescente numero di persone affette da patologie CV (2,3). Le malattie cerebrovascolari, in particolare, rappresentano la [more info]