Abstract
Le malattie cardiovascolari (CV) rappresentano la principale causa di mortalità nei paesi industrializzati. La riduzione dei livelli di colesterolo LDL (C-LDL) è fondamentale per la prevenzione degli eventi CV, soprattutto nei pazienti a rischio alto e molto alto. Le statine rappresentano il trattamento di prima linea per il controllo delle dislipidemie, ma molti pazienti non raggiungono i target lipidici raccomandati a causa di scarsa aderenza e tollerabilità. La terapia combinata di statina ed ezetimibe in un’unica compressa si è dimostrata una strategia efficace in termini di sicurezza, riduzione del C-LDL e miglioramento dell’aderenza terapeutica ed è raccomandata delle linee guida europee. La rosuvastatina, in particolare, si è dimostrata superiore rispetto ad altre statine (inclusa atorvastatina), sia in monoterapia che in combinazione con ezetimibe, offrendo una migliore riduzione del C-LDL con un minor rischio di effetti collaterali. L’uso di rosuvastatina ed ezetimibe in un’unica compressa rappresenta quindi un’opzione terapeutica ottimale per i pazienti ad alto rischio CV, consentendo una gestione più efficace e sicura della dislipidemia e un migliore controllo del rischio cardiovascolare.
Introduzione
Le malattie cardiovascolari (CV) rappresentano la principale causa di mortalità e disabilità nei paesi industrializzati occidentali. La prevenzione risulta fondamentale e deve essere promossa sia nella popolazione generale che nei soggetti a rischio, agendo sui fattori di rischio CV, tra cui i livelli circolanti di lipidi, la pressione arteriosa e il diabete. Riguardo ai lipidi, le recenti linee guida assegnano a ciascun livello di rischio CV un obiettivo terapeutico specifico relativo ai livelli di colesterolo LDL (C-LDL). Nei pazienti a rischio alto, l’obiettivo è ridurre il C-LDL a livelli inferiori a 70 mg/dL (<18 mmol/L), mentre nei pazienti a rischio molto alto, l’obiettivo è raggiungere livelli di C-LDL inferiori a 55 mg/dL (<14 mmol/L); in entrambi i casi è raccomandata inoltre una riduzione di almeno il 50% dei valori di C-LDL rispetto ai livelli basali (1). Studi randomizzati controllati e studi osservazionali hanno dimostrato che ridurre il C-LDL comporta una riduzione proporzionale del rischio CV, in particolare di quello coronarico (1). In questo contesto, l’approccio farmacologico è fondamentale per raggiungere gli obiettivi lipidici raccomandati e ridurre il rischio di eventi CV, soprattutto nei pazienti a rischio alto e molto alto (1).
La terapia farmacologica delle dislipidemie in pazienti a rischio alto/molto alto
L’avvento delle statine ha rivoluzionato la terapia farmacologica delle dislipidemie: numerosi trial clinici in prevenzione primaria e secondaria nel soggetto ad alto rischio CV hanno da tempo documentato efficacia e sicurezza di questa classe di farmaci (2–4), che rappresentano ora la terapia farmacologica di prima linea (1). Inoltre, vari studi hanno evidenziato come, nei pazienti a rischio molto alto, una terapia ipolipemizzante intensiva, avviata precocemente – entro pochi giorni – dopo un episodio di sindrome coronarica acuta (SCA), riduca maggiormente il rischio di eventi CV futuri rispetto ai regimi meno intensivi. Pertanto, nei pazienti con SCA, è raccomandato iniziare il trattamento ipolipemizzante già nel corso del ricovero ospedaliero e di proseguirlo indefinitamente, monitorando nel tempo il raggiungimento dell’obiettivo lipidico raccomandato (riduzione del C-LDL del 50% e <55mg/dl) (5). Un primo controllo dei livelli di C-LDL può essere eseguito dopo 4 settimane dalla dimissione o secondo quanto previsto dai protocolli diagnostico-terapeutici della struttura sanitaria di riferimento. Successivi controlli saranno stabiliti in base alle esigenze cliniche. Ad ogni visita di controllo, sarà necessario verificare la compliance del paziente e l’eventuale comparsa di effetti collaterali legati alla terapia ipolipemizzante.
Nonostante l’importanza di raggiungere i target terapeutici e implementare regimi intensivi, infatti, molti pazienti non riescono a raggiungere i livelli consigliati dalle linee guida (6,7). Le ragioni di questo scostamento dai target sono molteplici, includendo dosaggi inadeguati, scarsa continuità e scarsa implementazione della terapia, timori ingiustificati sugli effetti collaterali, e una ridotta aderenza. Inoltre, i pazienti a rischio alto e molto alto sono spesso anziani e affetti da più patologie, il che li porta a dover assumere numerosi farmaci quotidianamente. La necessità di seguire diverse terapie può contribuire alla scarsa aderenza al trattamento ipolipemizzante, aggravando ulteriormente le difficoltà nel raggiungere gli obiettivi lipidici raccomandati.
In Italia, l’aderenza e la persistenza nel trattamento con statine risultano particolarmente basse; le statine appartengono alle categorie terapeutiche con la più alta percentuale di scarsa aderenza (copertura terapeutica <40%), soprattutto nella fascia di età 65-84 anni (42,3%) (8). Allo stesso modo, la probabilità di interrompere il trattamento entro 150 giorni dall’inizio è del 50% (130 giorni per le donne, 180 giorni per gli uomini), con il picco massimo di interruzioni nella fascia 55-64 anni. Circa il 20% dei pazienti sospende la terapia dopo solo un mese, e solo un terzo dei nuovi utilizzatori continua il trattamento dopo un anno (38% degli uomini e 29% delle donne) (8). La scarsa aderenza e/o persistenza sono tra le principali cause di una risposta insufficiente alla terapia (9).
La terapia precostituita statina + ezetimibe
Considerando l’importanza di ridurre i livelli di C-LDL nel lungo termine, è essenziale scegliere un trattamento efficace sia in termini di effetti terapeutici che di aderenza, persistenza e sicurezza. In questo contesto, la terapia di combinazione precostituita in un’unica compressa contenente statina + ezetimibe assume particolare rilevanza. Tale strategia non solo ottimizza la riduzione del C-LDL, ma semplifica anche il regime terapeutico, migliorando l’aderenza e la persistenza del paziente e, di conseguenza, la gestione complessiva del rischio CV. Le stesse linee guida della Società Europea di Cardiologia raccomandano l’uso di farmaci che combinano più principi attivi in una singola compressa, in particolare l’associazione fissa tra una statina ad alta intensità e l’ezetimibe (1). Questa combinazione può ridurre il C-LDL del 65% circa e migliorare l’aderenza, soprattutto se somministrata in formulazioni precostituite (1,10,11). I pazienti che ricevono la combinazione statina + ezetimibe in una sola pillola hanno un’aderenza dell’87% maggiore rispetto a chi assume i due farmaci separatamente, indipendentemente da età, genere o profilo clinico, e con una riduzione degli outcomes cardiovascolari del 55% rispetto ai pazienti con bassa aderenza (11). La combinazione precostituita tra statine ed ezetimibe migliora gli outcomes clinici non solo tramite una migliore aderenza, ma anche tramite una maggiore efficacia in termini di effetto terapeutico. Una recente metanalisi ha dimostrato che una dose minima di statina ad elevata intensità (rosuvastatina 5mg/die), quando in combinazione con ezetimibe 10mg/die, è più efficace rispetto alla quadruplicazione della dose di statina (rosuvastatina fino a 20mg/die) (10).
Efficacia e sicurezza per la scelta della statina
L’entità della riduzione del C-LDL dipende dalla tipologia di statina più che dal relativo dosaggio, mentre gli eventi avversi dipendono più dal dosaggio che dal tipo di statina (1,12,13). Per questo motivo, la scelta della statina dovrebbe basarsi sulla possibilità di massimizzare l’effetto terapeutico minimizzando la dose del farmaco; le Linee Guida, per i pazienti a rischio alto e molto alto, raccomando sempre l’uso di una statina ad elevata intensità (1,12). Un regime ad alta intensità, in questo ambito, è definito come la dose di statina che, in media, riduce il C-LDL circolante di almeno il 50%; un regime ad intensità moderata è in grado di ridurlo del 30–50%, mentre uno a bassa intensità determina una riduzione al massimo pari al 30%. Sono considerate statine ad alta intensità, pertanto, solo rosuvastatina ed atorvastatina. La combinazione atorvastatina + ezetimibe, in due differenti dosaggi di statina è risultata essere estremamente efficace nel ridurre ulteriormente la LDL colesterolemia in pazienti provenienti da monoterapia statinica. Tuttavia, detta combinazione – pur estremamente efficace – lo è risultata significativamente meno rispetto alla combinazione rosuvastatina + ezetimibe in uno studio retrospettivo (14). Una metanalisi network conferma questo dato e mostra chiaramente la superiorità di rosuvastatina rispetto alle altre statine, compresa l’atorvastatina (15). I dati di questa metanalisi sostengono la superiorità di rosuvastatina e di rosuvastatina + ezetimibe nei confronti, rispettivamente, di tutte le altre statine considerate come monoterapia e delle altre combinazioni tra altre statine + ezetimibe. La rosuvastatina, inoltre, presenta un ottimale profilo farmacocinetico, risultando essere più sicura e tollerata, grazie alla sua elevata idrofilia (associata a selettività epatica con un minor rischio di effetti collaterali a livello muscolare) e al suo metabolismo che prevede l’eliminazione praticamente in forma immodificata per via biliare (minor rischio di interazioni farmaco-farmaco) (16).
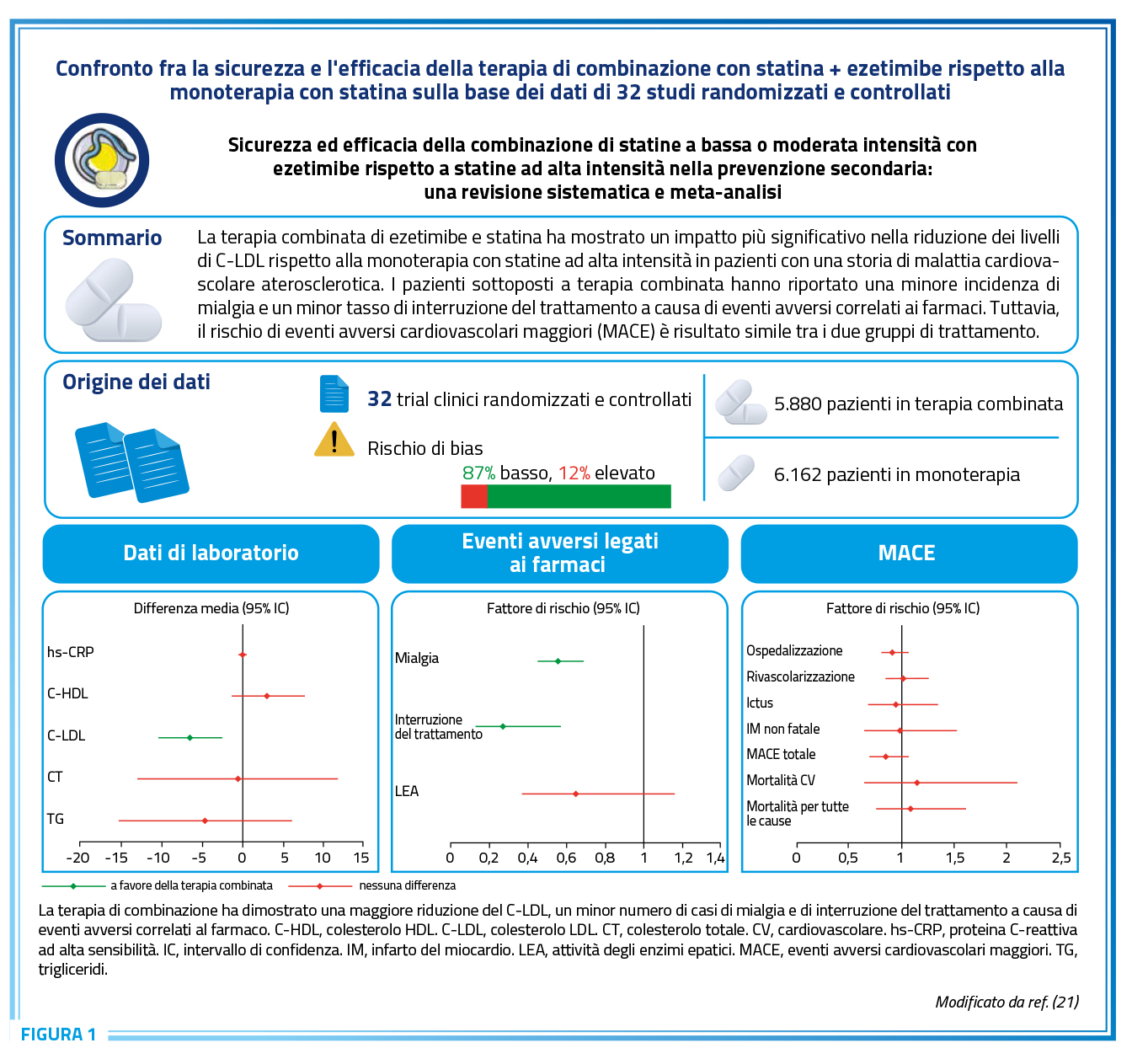
Un profilo di sicurezza adeguato è fondamentale per permettere al paziente di iniziare e mantenere la terapia nel lungo termine senza incorrere in gravi eventi avversi. La principale causa di interruzione della terapia con statine è infatti l’intolleranza, che riguarderebbe una percentuale variabile dal 10% al 30% dei pazienti (17,18) ed è spesso associata a sintomi muscolari (in inglese statin-associated muscle symptoms, SAMS), che risultano comunque infrequenti; il rischio di mialgia, inoltre, è minore con una terapia combinata con ezetimibe rispetto alla monoterapia (19). Diversi studi in doppio cieco suggeriscono che una parte significativa di questi eventi avversi, tuttavia, potrebbe essere legata a un effetto nocebo, con sintomi muscolari riportati solo quando i pazienti sono consapevoli di assumere una statina (17,20). Fra gli altri eventi avversi più comunemente riscontrati con le statine rientrano mal di testa, infezione delle vie respiratorie superiori, nausea, stanchezza e vertigini, mentre gli eventi gravi rimangono estremamente rari; in particolare, non sembrano esserci particolari differenze nell’incidenza di eventi avversi fra rosuvastatina e atorvastatina (19). Per quanto riguarda la persistenza, il rischio di interruzione del trattamento per eventi avversi è significativamente inferiore in coloro che ricevono la terapia di combinazione rispetto alla monoterapia, soprattutto nel caso di uso di rosuvastatina (21). In particolare, la probabilità di interrompere il trattamento a 12 mesi è del doppio per i regimi monoterapici rispetto a quelli in combinazione, così come mostrato da una recentissima review sistematica con metanalisi (Figura 1) (21).
Conclusione
In conclusione, la riduzione del C-LDL rappresenta un obiettivo cruciale per ridurre l’incidenza e la ricorrenza di eventi CV, particolarmente nei pazienti a rischio alto e molto alto. Tuttavia, il raggiungimento degli obiettivi lipidici risulta spesso difficoltoso a causa di terapie inadeguate e scarsamente implementate e, soprattutto, di una scarsa aderenza e persistenza al trattamento. In questo contesto, la combinazione di una statina con ezetimibe ha dimostrato una maggiore sicurezza e una migliore efficacia non solo nel ridurre significativamente i livelli di C-LDL, ma anche nel migliorare l’aderenza e la persistenza terapeutica, favorendo così una gestione ottimale del paziente. Tra le varie statine, la rosuvastatina si è dimostrata superiore sia in monoterapia che in combinazione con ezetimibe, garantendo risultati migliori in termini di effetto terapeutico, sicurezza, aderenza e persistenza rispetto ad altre statine, grazie anche ad un profilo farmacocinetico ottimale che la rende particolarmente adatta all’utilizzo nel paziente politrattato a rischio CV alto e molto alto.
Bibliografia
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111–88.
- Collins R, Armitage J, Parish S, Sleigh P, Peto R, Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol-lowering with simvastatin in 5963 people with diabetes: a randomised placebo-controlled trial. Lancet. 2003 Jun 14;361(9374):2005–16.
- Sever PS, Dahlöf B, Poulter NR, Wedel H, Beevers G, Caulfield M, et al. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial—Lipid Lowering Arm (ASCOT-LLA): a multicentre randomised controlled trial. The Lancet. 2003 Apr;361(9364):1149–58.
- Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, et al. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA. 2001 Apr 4;285(13):1711–8.
- De Luca L, Di Fusco SA, Iannopollo G, Mistrulli R, Rizzello V, Aimo A, et al. [ANMCO Scientific statement on combination therapies and polypill in secondary prevention]. G Ital Cardiol (Rome). 2024 May;25(5):367–81.
- Kristensen MS, Green A, Nybo M, Hede SM, Mikkelsen KH, Gislason G, et al. Lipid-lowering therapy and low-density lipoprotein cholesterol goal attainment after acute coronary syndrome: a Danish population-based cohort study. BMC Cardiovasc Disord. 2020 Jul 13;20(1):336.
- Ray KK, Haq I, Bilitou A, Manu MC, Burden A, Aguiar C, et al. Treatment gaps in the implementation of LDL cholesterol control among high- and very high-risk patients in Europe between 2020 and 2021: the multinational observational SANTORINI study. The Lancet regional health Europe. 2023 Jun;29:100624.
- Osservatorio Nazionale sull’impiego dei Medicinali. L’uso dei farmaci in Italia. Rapporto Nazionale Anno 2022. [Internet]. Rome; 2023 [cited 2024 Sep 12]. Available from: https://www.aifa.gov.it/ documents/20142/1967301/Rapporto-OsMed-2022.pdf
- Zhou Z, Curtis AJ, Breslin M, Nelson M. Letter by Zhou et al Regarding Article, “Statin Toxicity: Mechanistic Insights and Clinical Implications”. Circ Res. 2019 Jun 7;124(12):e120.
- Kang Y, Park JM, Lee SH. Moderate-Intensity Rosuvastatin/Ezetimibe Combination versus Quadruple-Dose Rosuvastatin Monotherapy: A Meta-Analysis and Systemic Review. Yonsei Med J. 2024 Jan;65(1):19–26.
- Rea F, Savaré L, Corrao G, Mancia G. Adherence to Lipid-Lowering Treatment by Single-Pill Combination of Statin and Ezetimibe. Adv Ther. 2021 Oct;38(10):5270–85.
- Grundy SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal RS, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the Management of Blood Cholesterol: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019 Jun 18;139(25):e1046–81.
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010 Nov 13;376(9753):1670–81.
- Lee J, Lee SH, Kim H, Lee SH, Cho JH, Lee H, et al. Low-density lipoprotein cholesterol reduction and target achievement after switching from statin monotherapy to statin/ezetimibe combination therapy: Real-world evidence. J Clin Pharm Ther. 2021 Feb;46(1):134–42.
- Zhang X, Xing L, Jia X, Pang X, Xiang Q, Zhao X, et al. Comparative Lipid-Lowering/Increasing Efficacy of 7 Statins in Patients with Dyslipidemia, Cardiovascular Diseases, or Diabetes Mellitus: Systematic Review and Network Meta-Analyses of 50 Randomized Controlled Trials. Cardiovasc Ther. 2020;2020:3987065.
- Bernini F, Catapano AL. [Rosuvastatin: pharmacologic features]. Ital Heart J. 2003 Dec;4 Suppl 7:22S-32S.
- Ward NC, Watts GF, Eckel RH. Statin Toxicity. Circ Res. 2019 Jan 18;124(2):328–50.
- Toth PP, Dayspring TD. Drug safety evaluation of rosuvastatin. Expert Opin Drug Saf. 2011 Nov;10(6):969–86.
- Zhang L, Zhang S, Yu Y, Jiang H, Ge J. Efficacy and safety of rosuvastatin vs. atorvastatin in lowering LDL cholesterol : A meta-analysis of trials with East Asian populations. Herz. 2020 Sep;45(6):594–602.
- Wood FA, Howard JP, Finegold JA, Nowbar AN, Thompson DM, Arnold AD, et al. N-of-1 Trial of a Statin, Placebo, or No Treatment to Assess Side Effects. New England Journal of Medicine. 2020 Nov 26;383(22):2182–4.
- Soleimani H, Mousavi A, Shojaei S, Tavakoli K, Salabat D, Farahani Rad F, et al. Safety and Effectiveness of High Intensity Statins Versus Low/Moderate Intensity Statins Plus Ezetimibe in Patients With Atherosclerotic Cardiovascular Disease for Reaching LDL C Goals: A Systematic Review and Meta Analysis. Clin Cardiol. 2024 Aug 12;47(8).
Abstract
Le malattie cardiovascolari (CV) rappresentano la principale causa di mortalità nei paesi industrializzati. La riduzione dei livelli di colesterolo LDL (C-LDL) è fondamentale per la prevenzione degli eventi CV, soprattutto nei pazienti a rischio alto e molto alto. Le statine rappresentano il trattamento di prima linea per il controllo delle dislipidemie, ma molti pazienti non raggiungono i target lipidici raccomandati a causa di scarsa aderenza e tollerabilità. La terapia combinata di statina ed ezetimibe in un’unica compressa si è dimostrata una strategia efficace in termini di sicurezza, riduzione del C-LDL e miglioramento dell’aderenza terapeutica ed è raccomandata delle linee guida europee. La rosuvastatina, in particolare, si è dimostrata superiore rispetto ad altre statine (inclusa atorvastatina), sia in monoterapia che in combinazione con ezetimibe, offrendo una migliore riduzione del C-LDL con un minor rischio di effetti collaterali. L’uso di rosuvastatina ed ezetimibe in un’unica compressa rappresenta quindi un’opzione terapeutica ottimale per i pazienti ad alto rischio CV, consentendo una gestione più efficace e sicura della dislipidemia e un migliore controllo del rischio cardiovascolare.
Introduzione
Le malattie cardiovascolari (CV) rappresentano la principale causa di mortalità e disabilità nei paesi industrializzati occidentali. La prevenzione risulta fondamentale e deve essere promossa sia nella popolazione generale che nei soggetti a rischio, agendo sui fattori di rischio CV, tra cui i livelli circolanti di lipidi, la pressione arteriosa e il diabete. Riguardo ai lipidi, le recenti linee guida assegnano a ciascun livello di rischio CV un obiettivo terapeutico specifico relativo ai livelli di colesterolo LDL (C-LDL). Nei pazienti a rischio alto, l’obiettivo è ridurre il C-LDL a livelli inferiori a 70 mg/dL (<18 mmol/L), mentre nei pazienti a rischio molto alto, l’obiettivo è raggiungere livelli di C-LDL inferiori a 55 mg/dL (<14 mmol/L); in entrambi i casi è raccomandata inoltre una riduzione di almeno il 50% dei valori di C-LDL rispetto ai livelli basali (1). Studi randomizzati controllati e studi osservazionali hanno dimostrato che ridurre il C-LDL comporta una riduzione proporzionale del rischio CV, in particolare di quello coronarico (1). In questo contesto, l’approccio farmacologico è fondamentale per raggiungere gli obiettivi lipidici raccomandati e ridurre il rischio di eventi CV, soprattutto nei pazienti a rischio alto e molto alto (1).
La terapia farmacologica delle dislipidemie in pazienti a rischio alto/molto alto
L’avvento delle statine ha rivoluzionato la terapia farmacologica delle dislipidemie: numerosi trial clinici in prevenzione primaria e secondaria nel soggetto ad alto rischio CV hanno da tempo documentato efficacia e sicurezza di questa classe di farmaci (2–4), che rappresentano ora la terapia farmacologica di prima linea (1). Inoltre, vari studi hanno evidenziato come, nei pazienti a rischio molto alto, una terapia ipolipemizzante intensiva, avviata precocemente – entro pochi giorni – dopo un episodio di sindrome coronarica acuta (SCA), riduca maggiormente il rischio di eventi CV futuri rispetto ai regimi meno intensivi. Pertanto, nei pazienti con SCA, è raccomandato iniziare il trattamento ipolipemizzante già nel corso del ricovero ospedaliero e di proseguirlo indefinitamente, monitorando nel tempo il raggiungimento dell’obiettivo lipidico raccomandato (riduzione del C-LDL del 50% e <55mg/dl) (5). Un primo controllo dei livelli di C-LDL può essere eseguito dopo 4 settimane dalla dimissione o secondo quanto previsto dai protocolli diagnostico-terapeutici della struttura sanitaria di riferimento. Successivi controlli saranno stabiliti in base alle esigenze cliniche. Ad ogni visita di controllo, sarà necessario verificare la compliance del paziente e l’eventuale comparsa di effetti collaterali legati alla terapia ipolipemizzante.
Nonostante l’importanza di raggiungere i target terapeutici e implementare regimi intensivi, infatti, molti pazienti non riescono a raggiungere i livelli consigliati dalle linee guida (6,7). Le ragioni di questo scostamento dai target sono molteplici, includendo dosaggi inadeguati, scarsa continuità e scarsa implementazione della terapia, timori ingiustificati sugli effetti collaterali, e una ridotta aderenza. Inoltre, i pazienti a rischio alto e molto alto sono spesso anziani e affetti da più patologie, il che li porta a dover assumere numerosi farmaci quotidianamente. La necessità di seguire diverse terapie può contribuire alla scarsa aderenza al trattamento ipolipemizzante, aggravando ulteriormente le difficoltà nel raggiungere gli obiettivi lipidici raccomandati.
In Italia, l’aderenza e la persistenza nel trattamento con statine risultano particolarmente basse; le statine appartengono alle categorie terapeutiche con la più alta percentuale di scarsa aderenza (copertura terapeutica <40%), soprattutto nella fascia di età 65-84 anni (42,3%) (8). Allo stesso modo, la probabilità di interrompere il trattamento entro 150 giorni dall’inizio è del 50% (130 giorni per le donne, 180 giorni per gli uomini), con il picco massimo di interruzioni nella fascia 55-64 anni. Circa il 20% dei pazienti sospende la terapia dopo solo un mese, e solo un terzo dei nuovi utilizzatori continua il trattamento dopo un anno (38% degli uomini e 29% delle donne) (8). La scarsa aderenza e/o persistenza sono tra le principali cause di una risposta insufficiente alla terapia (9).
La terapia precostituita statina + ezetimibe
Considerando l’importanza di ridurre i livelli di C-LDL nel lungo termine, è essenziale scegliere un trattamento efficace sia in termini di effetti terapeutici che di aderenza, persistenza e sicurezza. In questo contesto, la terapia di combinazione precostituita in un’unica compressa contenente statina + ezetimibe assume particolare rilevanza. Tale strategia non solo ottimizza la riduzione del C-LDL, ma semplifica anche il regime terapeutico, migliorando l’aderenza e la persistenza del paziente e, di conseguenza, la gestione complessiva del rischio CV. Le stesse linee guida della Società Europea di Cardiologia raccomandano l’uso di farmaci che combinano più principi attivi in una singola compressa, in particolare l’associazione fissa tra una statina ad alta intensità e l’ezetimibe (1). Questa combinazione può ridurre il C-LDL del 65% circa e migliorare l’aderenza, soprattutto se somministrata in formulazioni precostituite (1,10,11). I pazienti che ricevono la combinazione statina + ezetimibe in una sola pillola hanno un’aderenza dell’87% maggiore rispetto a chi assume i due farmaci separatamente, indipendentemente da età, genere o profilo clinico, e con una riduzione degli outcomes cardiovascolari del 55% rispetto ai pazienti con bassa aderenza (11). La combinazione precostituita tra statine ed ezetimibe migliora gli outcomes clinici non solo tramite una migliore aderenza, ma anche tramite una maggiore efficacia in termini di effetto terapeutico. Una recente metanalisi ha dimostrato che una dose minima di statina ad elevata intensità (rosuvastatina 5mg/die), quando in combinazione con ezetimibe 10mg/die, è più efficace rispetto alla quadruplicazione della dose di statina (rosuvastatina fino a 20mg/die) (10).
Efficacia e sicurezza per la scelta della statina
L’entità della riduzione del C-LDL dipende dalla tipologia di statina più che dal relativo dosaggio, mentre gli eventi avversi dipendono più dal dosaggio che dal tipo di statina (1,12,13). Per questo motivo, la scelta della statina dovrebbe basarsi sulla possibilità di massimizzare l’effetto terapeutico minimizzando la dose del farmaco; le Linee Guida, per i pazienti a rischio alto e molto alto, raccomando sempre l’uso di una statina ad elevata intensità (1,12). Un regime ad alta intensità, in questo ambito, è definito come la dose di statina che, in media, riduce il C-LDL circolante di almeno il 50%; un regime ad intensità moderata è in grado di ridurlo del 30–50%, mentre uno a bassa intensità determina una riduzione al massimo pari al 30%. Sono considerate statine ad alta intensità, pertanto, solo rosuvastatina ed atorvastatina. La combinazione atorvastatina + ezetimibe, in due differenti dosaggi di statina è risultata essere estremamente efficace nel ridurre ulteriormente la LDL colesterolemia in pazienti provenienti da monoterapia statinica. Tuttavia, detta combinazione – pur estremamente efficace – lo è risultata significativamente meno rispetto alla combinazione rosuvastatina + ezetimibe in uno studio retrospettivo (14). Una metanalisi network conferma questo dato e mostra chiaramente la superiorità di rosuvastatina rispetto alle altre statine, compresa l’atorvastatina (15). I dati di questa metanalisi sostengono la superiorità di rosuvastatina e di rosuvastatina + ezetimibe nei confronti, rispettivamente, di tutte le altre statine considerate come monoterapia e delle altre combinazioni tra altre statine + ezetimibe. La rosuvastatina, inoltre, presenta un ottimale profilo farmacocinetico, risultando essere più sicura e tollerata, grazie alla sua elevata idrofilia (associata a selettività epatica con un minor rischio di effetti collaterali a livello muscolare) e al suo metabolismo che prevede l’eliminazione praticamente in forma immodificata per via biliare (minor rischio di interazioni farmaco-farmaco) (16).
Un profilo di sicurezza adeguato è fondamentale per permettere al paziente di iniziare e mantenere la terapia nel lungo termine senza incorrere in gravi eventi avversi. La principale causa di interruzione della terapia con statine è infatti l’intolleranza, che riguarderebbe una percentuale variabile dal 10% al 30% dei pazienti (17,18) ed è spesso associata a sintomi muscolari (in inglese statin-associated muscle symptoms, SAMS), che risultano comunque infrequenti; il rischio di mialgia, inoltre, è minore con una terapia combinata con ezetimibe rispetto alla monoterapia (19). Diversi studi in doppio cieco suggeriscono che una parte significativa di questi eventi avversi, tuttavia, potrebbe essere legata a un effetto nocebo, con sintomi muscolari riportati solo quando i pazienti sono consapevoli di assumere una statina (17,20). Fra gli altri eventi avversi più comunemente riscontrati con le statine rientrano mal di testa, infezione delle vie respiratorie superiori, nausea, stanchezza e vertigini, mentre gli eventi gravi rimangono estremamente rari; in particolare, non sembrano esserci particolari differenze nell’incidenza di eventi avversi fra rosuvastatina e atorvastatina (19). Per quanto riguarda la persistenza, il rischio di interruzione del trattamento per eventi avversi è significativamente inferiore in coloro che ricevono la terapia di combinazione rispetto alla monoterapia, soprattutto nel caso di uso di rosuvastatina (21). In particolare, la probabilità di interrompere il trattamento a 12 mesi è del doppio per i regimi monoterapici rispetto a quelli in combinazione, così come mostrato da una recentissima review sistematica con metanalisi (Figura 1) (21).
Conclusione
In conclusione, la riduzione del C-LDL rappresenta un obiettivo cruciale per ridurre l’incidenza e la ricorrenza di eventi CV, particolarmente nei pazienti a rischio alto e molto alto. Tuttavia, il raggiungimento degli obiettivi lipidici risulta spesso difficoltoso a causa di terapie inadeguate e scarsamente implementate e, soprattutto, di una scarsa aderenza e persistenza al trattamento. In questo contesto, la combinazione di una statina con ezetimibe ha dimostrato una maggiore sicurezza e una migliore efficacia non solo nel ridurre significativamente i livelli di C-LDL, ma anche nel migliorare l’aderenza e la persistenza terapeutica, favorendo così una gestione ottimale del paziente. Tra le varie statine, la rosuvastatina si è dimostrata superiore sia in monoterapia che in combinazione con ezetimibe, garantendo risultati migliori in termini di effetto terapeutico, sicurezza, aderenza e persistenza rispetto ad altre statine, grazie anche ad un profilo farmacocinetico ottimale che la rende particolarmente adatta all’utilizzo nel paziente politrattato a rischio CV alto e molto alto.
Bibliografia
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111–88.
- Collins R, Armitage J, Parish S, Sleigh P, Peto R, Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol-lowering with simvastatin in 5963 people with diabetes: a randomised placebo-controlled trial. Lancet. 2003 Jun 14;361(9374):2005–16.
- Sever PS, Dahlöf B, Poulter NR, Wedel H, Beevers G, Caulfield M, et al. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial—Lipid Lowering Arm (ASCOT-LLA): a multicentre randomised controlled trial. The Lancet. 2003 Apr;361(9364):1149–58.
- Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, et al. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA. 2001 Apr 4;285(13):1711–8.
- De Luca L, Di Fusco SA, Iannopollo G, Mistrulli R, Rizzello V, Aimo A, et al. [ANMCO Scientific statement on combination therapies and polypill in secondary prevention]. G Ital Cardiol (Rome). 2024 May;25(5):367–81.
- Kristensen MS, Green A, Nybo M, Hede SM, Mikkelsen KH, Gislason G, et al. Lipid-lowering therapy and low-density lipoprotein cholesterol goal attainment after acute coronary syndrome: a Danish population-based cohort study. BMC Cardiovasc Disord. 2020 Jul 13;20(1):336.
- Ray KK, Haq I, Bilitou A, Manu MC, Burden A, Aguiar C, et al. Treatment gaps in the implementation of LDL cholesterol control among high- and very high-risk patients in Europe between 2020 and 2021: the multinational observational SANTORINI study. The Lancet regional health Europe. 2023 Jun;29:100624.
- Osservatorio Nazionale sull’impiego dei Medicinali. L’uso dei farmaci in Italia. Rapporto Nazionale Anno 2022. [Internet]. Rome; 2023 [cited 2024 Sep 12]. Available from: https://www.aifa.gov.it/ documents/20142/1967301/Rapporto-OsMed-2022.pdf
- Zhou Z, Curtis AJ, Breslin M, Nelson M. Letter by Zhou et al Regarding Article, “Statin Toxicity: Mechanistic Insights and Clinical Implications”. Circ Res. 2019 Jun 7;124(12):e120.
- Kang Y, Park JM, Lee SH. Moderate-Intensity Rosuvastatin/Ezetimibe Combination versus Quadruple-Dose Rosuvastatin Monotherapy: A Meta-Analysis and Systemic Review. Yonsei Med J. 2024 Jan;65(1):19–26.
- Rea F, Savaré L, Corrao G, Mancia G. Adherence to Lipid-Lowering Treatment by Single-Pill Combination of Statin and Ezetimibe. Adv Ther. 2021 Oct;38(10):5270–85.
- Grundy SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal RS, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the Management of Blood Cholesterol: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019 Jun 18;139(25):e1046–81.
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010 Nov 13;376(9753):1670–81.
- Lee J, Lee SH, Kim H, Lee SH, Cho JH, Lee H, et al. Low-density lipoprotein cholesterol reduction and target achievement after switching from statin monotherapy to statin/ezetimibe combination therapy: Real-world evidence. J Clin Pharm Ther. 2021 Feb;46(1):134–42.
- Zhang X, Xing L, Jia X, Pang X, Xiang Q, Zhao X, et al. Comparative Lipid-Lowering/Increasing Efficacy of 7 Statins in Patients with Dyslipidemia, Cardiovascular Diseases, or Diabetes Mellitus: Systematic Review and Network Meta-Analyses of 50 Randomized Controlled Trials. Cardiovasc Ther. 2020;2020:3987065.
- Bernini F, Catapano AL. [Rosuvastatin: pharmacologic features]. Ital Heart J. 2003 Dec;4 Suppl 7:22S-32S.
- Ward NC, Watts GF, Eckel RH. Statin Toxicity. Circ Res. 2019 Jan 18;124(2):328–50.
- Toth PP, Dayspring TD. Drug safety evaluation of rosuvastatin. Expert Opin Drug Saf. 2011 Nov;10(6):969–86.
- Zhang L, Zhang S, Yu Y, Jiang H, Ge J. Efficacy and safety of rosuvastatin vs. atorvastatin in lowering LDL cholesterol : A meta-analysis of trials with East Asian populations. Herz. 2020 Sep;45(6):594–602.
- Wood FA, Howard JP, Finegold JA, Nowbar AN, Thompson DM, Arnold AD, et al. N-of-1 Trial of a Statin, Placebo, or No Treatment to Assess Side Effects. New England Journal of Medicine. 2020 Nov 26;383(22):2182–4.
- Soleimani H, Mousavi A, Shojaei S, Tavakoli K, Salabat D, Farahani Rad F, et al. Safety and Effectiveness of High Intensity Statins Versus Low/Moderate Intensity Statins Plus Ezetimibe in Patients With Atherosclerotic Cardiovascular Disease for Reaching LDL C Goals: A Systematic Review and Meta Analysis. Clin Cardiol. 2024 Aug 12;47(8).
Related papers
La pubblicazione recente di alcuni lavori scientifici basati sulle risultanze di alcuni osservatori epidemiologi mondiali, ha riportato alla ribalta il ruolo chiave delle malattie cardiovascolari come prima causa di morte e disabilità, non solo nel presente, ma anche nel futuro proiettato oggi al 2050 con un incremento più o meno equamente distribuito tra le malattie [more info]
1) Lipoproteine ed aterosclerosi Le lipoproteine sono particelle composte da un nucleo ricco in esteri del colesterolo e trigliceridi (TG) circondati da colesterolo libero, fosfolipidi e apolipoproteine. Le lipoproteine plasmatiche vengono suddivise in varie classi (VLDL, IDL, LDL, HDL e chilomicroni) in base alle dimensioni, alla composizione lipidica e alle apolipoproteine presenti (Tabella 1). I [more info]
Introduzione Le malattie cardiovascolari rappresentano la principale causa di morbilità e mortalità a livello globale, nonostante i progressi nella prevenzione e nel trattamento farmacologico. In questo contesto, l’adozione di strategie terapeutiche efficaci per la gestione dei fattori di rischio cardiovascolare è fondamentale. La combinazione farmacologica di farmaci con meccanismi d’azione complementari è diventata una pratica [more info]