Introduzione
Malgrado la riduzione dell’incidenza e prevalenza delle coronaropatie negli ultimi 30 anni in tutti i paesi industrializzati dell’occidente, la patologia cardiovascolare rimane la causa principale di mortalità e di invalidità. Il progressivo invecchiamento della popolazione, il costante aumento del diabete e di alcuni fattori di rischio quali l’obesità e l’ipertensione arteriosa, aumenteranno ulteriormente l’incidenza, la prevalenza e il carico assistenziale ed economico legato alla patologia cardiovascolare, non solo nei paesi industrializzati ma anche nei paesi in via di sviluppo.
In Italia le malattie dell’apparato cardiovascolare sono la prima causa di morte nel complesso della popolazione e tra gli anziani, e la seconda tra gli adulti, subito dopo i tumori (1).
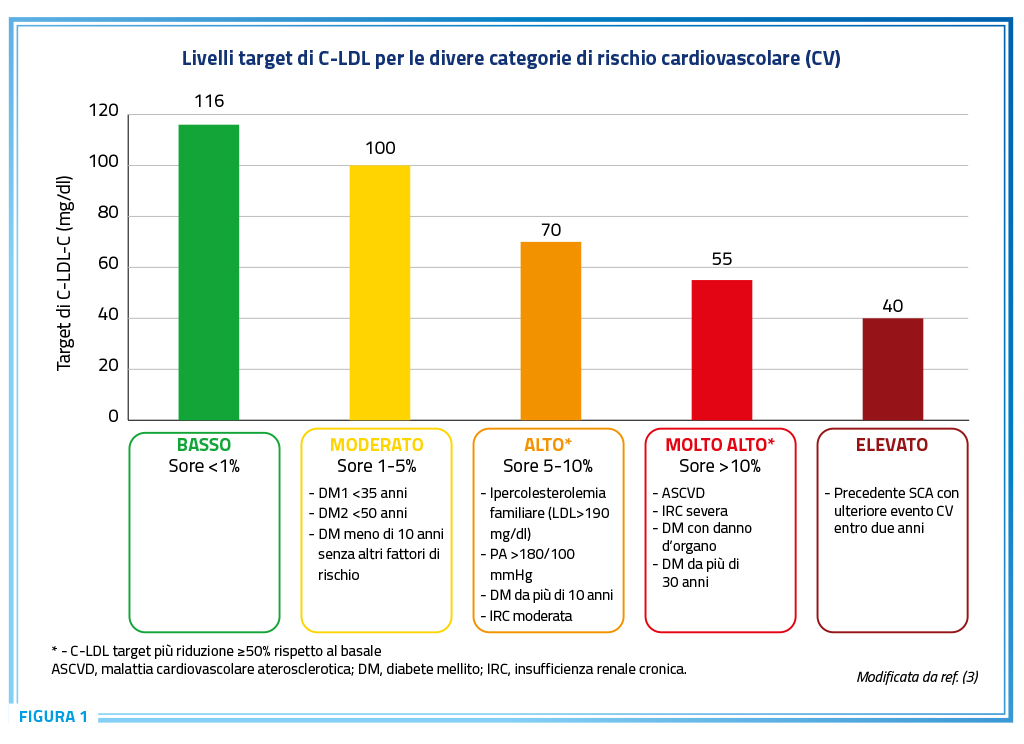
L’importanza della prevenzione cardiovascolare (CV) rimane indiscussa e deve essere promossa a diversi livelli, sia nella popolazione generale, attraverso la promozione di comportamenti e stili di vita sani sia a livello individuale soprattutto nei soggetti a medio ed alto rischio agendo sui fattori di rischio cardiovascolare, tra i quali i livelli lipidici, la pressione arteriosa e il diabete. Le nuove linee guida confermano che l’approccio al paziente parte dalla stratificazione in classi di rischio, a ciascuna delle quali viene assegnato un obiettivo terapeutico in termini di livelli di colesterolo LDL (C-LDL) secondo cui più basso è il livello di C-LDL, migliore è la prevenzione CV. In linea generale, i soggetti ad alto rischio dovrebbero essere identificati e gestiti prontamente. Le raccomandazioni indicano, per i pazienti a rischio molto alto (sia in prevenzione primaria che in quella secondaria), l’obiettivo di C-LDL <55 mg/dL (<1,4 mmol/L) e almeno il 50% di riduzione dei livelli basali. Nei pazienti ad alto rischio, l’obiettivo di C-LDL è <70 mg/dL (o <1,8 mmol/L) e almeno il 50% di riduzione dai livelli basali (Figura 1) (2, 3). La correlazione tra i livelli del colesterolo plasmatico e il rischio cardiovascolare è definita da una serie ormai ricca di studi osservazionali prospettici, condotti in varie aree del mondo; il nesso causale (e non semplicemente di associazione) tra questi due parametri è confermato dai risultati dei numerosi studi di intervento, randomizzati e controllati, che hanno documentato come la riduzione della colesterolemia stessa, ottenuta mediante interventi di varia natura (soprattutto di natura farmacologica), induca una proporzionale riduzione del rischio cardiovascolare e soprattutto coronarico. Questo complesso di evidenze, che si è andato accumulando nella letteratura scientifica, è stato integrato da una crescente attenzione alla caratterizzazione del paziente candidato all’intervento ipocolesterolemizzante, essenzialmente basata sulla stima del suo rischio cardiovascolare globale, e dalla definizione dell’ampiezza del calo dell’LDL o del valore obiettivo (target) da perseguire, mediante l’intervento terapeutico (3).
Un’efficace terapia farmacologica ipolipemizzante, quando la correzione degli stili di vita non risulti sufficiente, può prevenire lo sviluppo di coronaropatia e ridurre significativamente l’incidenza di eventi coronarici e cerebrovascolari.
L’avvento delle statine ha rivoluzionato la terapia farmacologica delle dislipidemie: numerosi trial clinici in prevenzione primaria e secondaria, nel soggetto ad alto rischio, nel paziente anziano, nel diabetico, nell’iperteso e nelle sindromi coronariche acute hanno documentato efficacia e sicurezza di questa classe farmacologica (4-6).
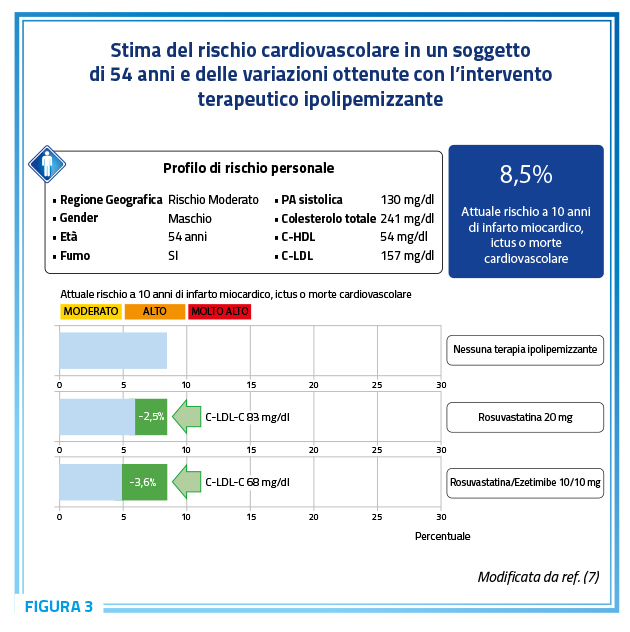
Ad oggi è possibile eseguire una gestione personalizzata del rischio cardiovascolare con idonei calcolatori. Ad esempio, il sito U-Prevent rappresenta un supporto alle decisioni cliniche certificato, attraverso l’inserimento dei dati clinici del paziente e dell’area geografia, per determinare un profilo di rischio individuale di sviluppare la malattia cardiovascolare e valutare le modifiche del rischio cardiovascolare ottenute con l’intervento terapeutico (7) (Figura 2).
Le Linee Guida
Le linee guida per la gestione della colesterolemia che si sono succedute negli ultimi vent’anni, hanno sottolineato come l’elemento che più si è modificato è l’obiettivo terapeutico degli interventi di controllo della colesterolemia. A partire dall’ormai storico documento denominato ATP-III, che nel 2001 suggeriva di portare la colesterolemia LDL dei soggetti in prevenzione secondaria, o portatori di “equivalenti coronarici” (arteriopatia obliterante degli arti inferiori, aneurisma dell’aorta addominale, malattia carotidea sintomatica), a un valore inferiore a 100 mg/dl, i documenti successivi, sia negli Stati Uniti sia in Europa, hanno indicato valori target progressivamente decrescenti. Nei soggetti con eventi recidivanti nonostante l’istituzione di un’efficace terapia ipocolesterolemizzante, l’obiettivo terapeutico per la colesterolemia LDL è ulteriormente ridotto a 40 mg/dl, quindi risulta ampliato il numero dei pazienti candidati a interventi più aggressivi su questo parametro, e la necessità di utilizzare più ampliamente farmaci a elevata efficacia (3).
Ruolo fondamentale è giocato anche dalla tempestività dell’inizio del trattamento. Diversi studi hanno dimostrato che l’adozione di una terapia ipolipemizzante intensiva entro 10 giorni da un episodio di SCA riduca il rischio in misura maggiore rispetto a regimi non intensivi. È raccomandabile iniziare sin dalla dimissione un trattamento con statina ad elevata intensità ed ezetimibe, in associazioni precostituite (8). La terapia ipolipemizzante deve continuare indefinitamente dopo la dimissione, avendo cura di verificare il raggiungimento e il mantenimento del target lipidico raccomandato nel tempo (C-LDL ridotto del 50% e <55mg/dl). Un primo controllo del C-LDL potrà essere effettuato dopo 4 settimane dalla dimissione, oppure secondo quanto previsto nei percorsi diagnostico-terapeutici assistenziali vigenti presso la singola struttura. Successivi controlli dovranno essere definiti in rapporto alle esigenze cliniche. In occasione di ogni controllo dovrà essere verificata l’aderenza del paziente alle prescrizioni e l’eventuale comparsa di effetti collaterali o reazioni avverse correlabili alla terapia ipolipemizzante.
A tal proposito, risulta importante non soltanto raggiungere i target terapeutici definiti a seconda dei profili di rischio e del grado di prevenzione, ma attuare un regime terapeutico il più intensivo possibile in modo tempestivo. Malgrado ciò numerosi pazienti in trattamento con questi farmaci non raggiungono di fatto il target terapeutico individuato dalle varie linee guida.
Tuttavia, nonostante le raccomandazioni delle linee guida, i dati di “real world” continuano a porre in evidenza le difficoltà a raggiungere i target indicati (9). A tal proposito, lo studio SANTORINI è uno studio multinazionale, prospettico, osservazionale, che fino ad oggi ha arruolato più di 9.500 pazienti da più di 800 centri in 14 Paesi in tutta Europa. I primi risultati mostrano che, al basale, il 18,6% dei pazienti a rischio cardiovascolare alto e molto alto non riceveva alcuna terapia ipolipemizzante (LLT). La maggior parte dei pazienti (54,1%) ha ricevuto LLT in monoterapia, e le terapie di associazione sono state utilizzate solo nel 27,3% dei pazienti. Esso dimostra e conferma la necessità di rivalutare e ripensare gli approcci per gestire i livelli di colesterolo nei pazienti ad alto e altissimo rischio di malattie cardiovascolari, assicurando in particolare che questi pazienti ricevano le terapie ipolipemizzanti più appropriate per tipo e dosaggio (10).
L’analisi dei dati dello studio START (in inglese STable Coronary Artery Diseases RegisTry) mostra un raggiungimento subottimale dei valori target di C-LDL nei pazienti a rischio cardiovascolare molto alto: valori di C-LDL <70 mg/dl sono ottenuti solo nel 58,1% dei pazienti, mentre solo il 3,2% raggiunge concentrazioni sieriche <55 mg/dl (11). Questo risultato sembra essere correlato anche ai potenziali eventi avversi legati alle statine (mialgie, dolori articolari, astenia, ecc.) che possono manifestarsi in 50-100 casi ogni 10.000 pazienti trattati per 5 anni. Ne consegue un sottoutilizzo dei farmaci ipolipemizzanti in pazienti ad alto rischio, con gravi ripercussioni sulla sopravvivenza e la qualità di vita degli stessi (12).
Le cause di questo gap tra target previsto dalle linee guida e target concretamente raggiunto nel “mondo reale” derivano probabilmente da numerosi fattori, quali ad esempio una terapia incongrua per dosaggio e continuità di somministrazione, una spesso ingiustificata paura di effetti collaterali, una inadeguata compliance da parte dei pazienti, ma anche dall’obiettiva difficoltà nel riuscire ad abbassare il colesterolo totale e LDL ai livelli consigliati dalle linee guida.
La terapia farmacologica delle dislipidemie
Le statine esercitano il loro effetto principale con la riduzione dei livelli di colesterolo LDL, inibendo competitivamente la HMG-CoA riduttasi e, di conseguenza, la sintesi endogena di colesterolo a livello epatico. La ridotta disponibilità di colesterolo cellulare determina un aumento dell’espressione sulla superficie degli epatociti del gene del recettore per le LDL che porta ad una aumentata rimozione delle LDL circolanti, riducendo così i livelli plasmatici del C-LDL.
La monoterapia con le statine è in genere ben tollerata, anche se con una frequenza non trascurabile si assiste alla comparsa di eventi avversi, i più importanti dei quali sono la miopatia e un aumento asintomatico delle transaminasi epatiche, nonché possibili interazioni con altri farmaci.
La rosuvastatina sembrerebbe rispondere positivamente alla maggior parte di questi requisiti, per la sua efficacia nel correggere simultaneamente le diverse alterazioni del profilo lipidico, per la sua efficacia di riduzione del C-LDL anche alle dosi più basse e quindi senza necessità di ulteriori adeguamenti, per i minimi rischi di interferenza con altri farmaci abitualmente utilizzati in associazione alle statine. Si tratta, in effetti, della molecola più efficace nel ridurre la colesterolemia tra le statine attualmente disponibili in Europa (13). La dose giornaliera varia da 5 a 40 mg. Dopo somministrazione per via orale la rosuvastatina viene ben assorbita dal tratto gastroenterico e la concentrazione plasmatica di picco viene raggiunta entro circa 5 ore dalla assunzione. La molecola è idrosolubile e presenta una biodisponibilità assoluta pari a circa il 20%. L’eliminazione avviene in forma immodificata nelle feci (90% circa), mentre la parte rimanente viene escreta nelle urine. L’emivita del farmaco è di circa 19 ore (14) consentendo l’eventuale assunzione ad inizio giornata.
Tuttavia, recenti evidenze, al fine di migliorare l’aderenza terapeutica grazie ad una riduzione degli effetti indesiderati secondari all’utilizzo di statina ad alta intensità, propongono di associare ad una statina ad intensità moderata l’ezetimibe. L’ezetimibe riduce significativamente la colesterolemia LDL anche in pazienti già in terapia con statina, essa porta ad un ulteriore e significativo beneficio clinico; inoltre, presenta altre azioni “antiaterosclerotiche” modulando il contenuto degli steroli vegetali e correggendo la disfunzione endoteliale.
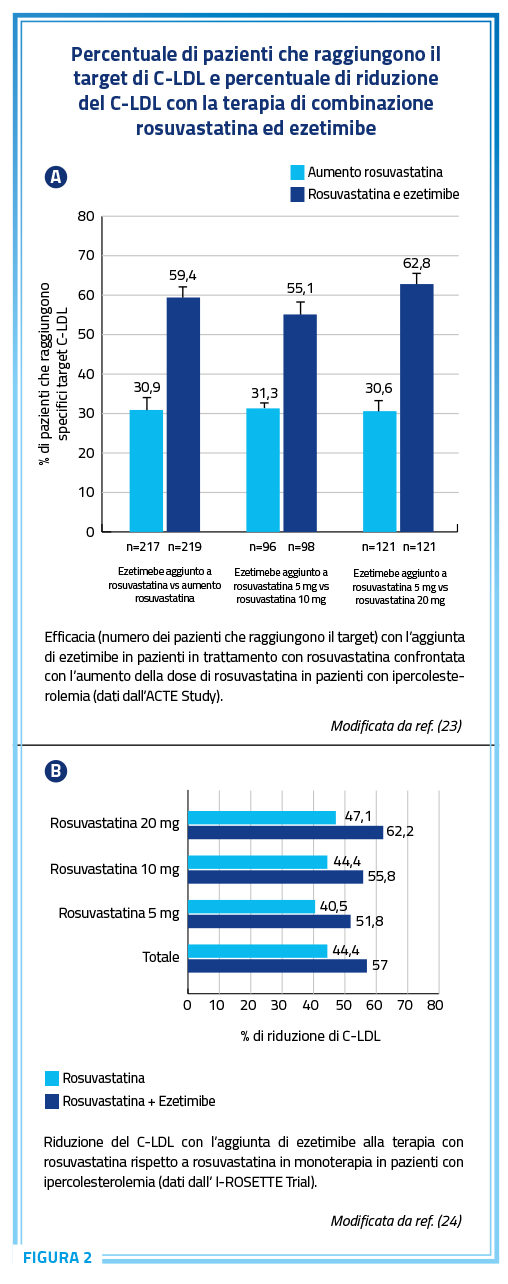
Il diverso meccanismo d’azione di statine ed ezetimibe rende questi approcci terapeutici complementari nel ridurre i livelli di C-LDL e rappresenta il razionale per un loro impiego in associazione. Studi osservazionali hanno riportato che con l’uso delle statine in combinazione con ezetimibe i target terapeutici si ottengono con maggiore probabilità (rispettivamente il 21% e 58% dei pazienti raggiunge i valori raccomandati dalle ultime linee guida). Diverse evidenze hanno mostrato come, sia in termini di raggiungimento dei livelli target di C-LDL che di miglioramento di tutti i parametri lipidici considerati, sia più vantaggioso l’impiego della terapia di combinazione statina-ezetimibe, piuttosto che raddoppiare la dose iniziale di statina. Sulla base delle evidenze accumulate, le linee guida indicano la terapia di associazione come strategia terapeutica appropriata nei pazienti a rischio alto e molto alto che non raggiungono i target con la monoterapia. La combinazione della statina alla massima dose tollerata con l’ezetimibe viene indicata come prima opzione terapeutica, in particolare, nei pazienti a rischio molto elevato, così come quelli a rischio estremamente elevato (1 o più eventi entro 2 anni), potrebbe essere vantaggioso iniziare la terapia ipolipemizzante direttamente con la combinazione statine ed ezetimibe. Va anche rilevato che i meccanismi d’azione complementari di rosuvastatina e di ezetimibe, attivi, la prima sulla sintesi epatica del colesterolo e il secondo sul suo assorbimento intestinale, consentono di ottenere una risposta terapeutica, nei singoli individui, molto omogenea.
L’aggiunta di ezetimibe, al dosaggio standard di 10 mg/die, a una statina induce un calo aggiuntivo della colesterolemia dell’ordine del 18-20%, con un effetto complessivo sulla colesterolemia LDL pari a quello ottenibile se il dosaggio della statina venisse aumentato di otto volte, secondo la ben nota “regola del 6%”, senza indurre l’aumento del rischio di effetti collaterali (15) (Figura 3). Studi che hanno esaminato l’efficacia di rosuvastatina versus atorvastatina hanno evidenziato come la rosuvastatina sia più efficace nella rapida stabilizzazione della placca e di una maggiore regressione del suo volume (16) a fronte anche di un miglior rapporto apoB/ApoA1 lipoproteina (17).
La terapia di combinazione
Le osservazioni del mondo reale, tuttavia, attestano l’ampio divario circa l’effettivo conseguimento dei target raccomandati dalle linee guida. Nello studio osservazionale europeo DA VINCI solo il 18% dei 2.888 pazienti in prevenzione secondaria presentava un valore di C-LDL <55 mg/dl, di questi solo il 9% era in trattamento con statina a moderata/alta intensità + ezetimibe e il 45,8% era in trattamento con una statina a bassa o media intensità (18).
Questo potrebbe essere spiegato in parte dallo scarso impiego di terapie di combinazione, in parte dalla bassa aderenza al trattamento, ascrivibile, tra i diversi fattori, alla terapia poli-farmacologica stessa che impone al paziente con multiple comorbilità l’assunzione di diversi farmaci. La polipillola, contenente diversi agenti farmacologici mirati al controllo di uno o più fattori di rischio o di malattia, rappresenta una strategia di semplificazione della terapia che consente di favorire l’aderenza e migliorare gli outcomes clinici cardiovascolari (19).
Una revisione sistematica della letteratura, che ha incluso nove studi clinici randomizzati, ha evidenziato che una polipillola contenente almeno un agente antipertensivo e uno ipocolesterolemizzante è associata ad un’aderenza terapeutica del 33% superiore rispetto alla terapia standard (20). Ad oggi, le linee guida della Societa Europea di Cardiologia sulla gestione delle dislipidemie raccomandano l’impiego di farmaci che contengono più agenti terapeutici in un’unica compressa. Il peso della polifarmacologia sull’aderenza terapeutica è confermato anche dalla dimostrazione che i pazienti in terapia ipolipemizzante che ricevono l’associazione statina + ezetimibe in un’unica pillola presentano una probabilità dell’87% più elevata di essere altamente aderenti al trattamento rispetto a quelli che assumono i due farmaci separatamente, indipendentemente da età, genere o profilo clinico, e con una riduzione degli outcomes cardiovascolari del 55% rispetto ai pazienti con bassa aderenza (21).
Aggiungere ezetimibe ad una statina a dose fissa in una singola pillola aumenta l’aderenza terapeutica. La vera o presunta intolleranza e le non infrequenti riferite mialgie nei pazienti in terapia con statine, specialmente se lipofile e ad alte dosi, influenza grandemente l’aderenza terapeutica con conseguenze anche gravi sulla prognosi. L’adesione terapeutica risulta essere, probabilmente, la sfida più moderna e difficile per il medico e un primo passo concreto potrebbe essere quello di “semplificare” il più possibile la prescrizione terapeutica, utilizzando le combinazioni farmacologiche.
In conclusione, tali osservazioni suggeriscono che la terapia di associazione a dosi fisse e in una singola pillola determini non solo un più efficiente controllo dei livelli di C-LDL ed un possibile miglioramento degli outcomes con una significativa riduzione degli effetti collaterali, ma soprattutto un rilevante aumento dell’aderenza terapeutica, rinforzando sempre più in maniera convincente il potenziale ruolo della terapia di combinazione anche nella fase immediatamente post-acuta della sindrome coronarica acuta (SCA).
Terapie ipolipemizzanti e aderenza
Tra le diverse azioni implementate per migliorare l’aderenza, quelle che si sono rivelate maggiormente costo-efficaci e dunque in grado di incidere in maniera significativa sulla riduzione dei costi sanitari, sono rappresentate dagli interventi educativi rivolti ai pazienti e al personale sanitario, l’utilizzo di farmaci in associazione fissa o di polipillole che consentono di semplificare la terapia, il coinvolgimento delle farmacie e del personale sanitario, la riduzione della spesa out-of-pocket e il monitoraggio dell’aderenza tramite interventi ad hoc.
Indiscutibilmente la semplificazione degli schemi terapeutici rappresenta uno degli interventi più efficaci per migliorare l’aderenza terapeutica. Il frazionamento delle dosi di farmaco e la complessità dello schema terapeutico, infatti, impattano negativamente sull’aderenza (22).
Non sorprende, quindi, l’interesse che la letteratura scientifica ha rivolto nel corso degli anni all’uso in prevenzione cardiovascolare di combinazioni precostituite di farmaci, della stessa classe o di classi diverse, che consentissero da un lato di semplificare gli schemi terapeutici attraverso la riduzione del numero di compresse e dall’altro di massimizzare la resa preventiva sfruttando le sinergie farmacologiche. Le sinergie terapeutiche rappresentano senza dubbio uno strumento prezioso per il clinico in quanto consentono di raggiungere target terapeutici ambiziosi utilizzando combinazioni razionali di farmaci.
Conclusioni
Quando è presente ipercolesterolemia, dobbiamo porci alcune domande: chi è il paziente? Qual è il suo rischio cardiovascolare globale? Qual è il suo target di C-LDL? Quale terapia farmacologica? Alla luce di questi quesiti, occorre conoscere prima di tutto la storia clinica personale e familiare del paziente, i suoi dati ematochimici e il suo profilo lipidico.
Le più recenti linee guida internazionali, sulla base dei risultati degli studi di osservazione e di intervento disponibili in letteratura, propongono obiettivi terapeutici molto ambiziosi, in linea con la filosofia “the lower, the better”. Ne discende l’esigenza di ridurre spesso in maniera molto marcata la colesterolemia LDL, soprattutto nei pazienti ad alto o altissimo rischio. La disponibilità di una combinazione a dosaggio fisso tra rosuvastatina ed ezetimibe consente di affrontare e risolvere, in un numero significativo di pazienti, il problema della riduzione della colesterolemia LDL. Sono soprattutto importanti, al proposito, l’ampio effetto sulla colesterolemia LDL, l’elevata tollerabilità (soprattutto in termini di basso rischio di interazioni farmacologiche), l’elevata prevedibilità della risposta terapeutica a questa combinazione, dovuta alla contemporanea presenza di molecole con effetti sulla sintesi ma anche sull’assorbimento del colesterolo, e – non ultimo – il costo contenuto.
Le più recenti evidenze scientifiche enfatizzano l’efficacia della polipillola nella prevenzione cardiovascolare, integrando con successo il concetto di semplificazione terapeutica con una sinergia di efficacia protettiva. Questo approccio moderno rappresenta un tassello imprescindibile per la gestione ottimale del paziente cardiovascolare.
Bibliografia
- Clinical trials with rosuvastatin: efficacy and safety of its use Schweiger C. Ital Heart J. 2003 Dec;4 Suppl 7:33S-46S.
- Cholesterol Treatment Trialists’ – CTT – Collaboration. Efficacy and safety of LDL-lowering therapy among men and women: meta-analysis of individual data from 174 000 participants in 27 randomised trials. Lancet 2015; 385:1397-405.
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188.
- Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 5963 people with diabetes: a randomised placebo controlled trial. Lancet 2003; 361: 2005-16.
- Sever PS, Dahlöf B, Poulter NR, Wedel H, Beevers G, Caulfield M, Collins R, Kjeldsen SE, Kristinsson A, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, Ostergren J; ASCOT investigators. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial–Lipid Lowering Arm (ASCOT-LLA): a multicentre randomised controlled trial. Lancet. 2003 Apr 5;361(9364):1149-58.
- Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, Zeiher A, Chaitman BR, Leslie S, Stern T; Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) Study Investigators. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA. 2001 Apr 4;285(13):1711-8.
- U-Prevent site powered by ORTEC. Version: 293. https://u-prevent.com/
- De Luca L, Di Fusco SA, Iannopollo G, Mistrulli R, Rizzello V, Aimo A, Navazio A, Bilato C, Corda M, Di Marco M, Geraci G, Iacovoni A, Milli M, Pascale V, Riccio C, Scicchitano P, Tizzani E, Gabrielli D, Grimaldi M, Colivicchi F, Oliva F. Scientific statement ANMCO sulla semplificazione del regime terapeutico farmacologico in prevenzione secondaria. G Ital Cardiol 2024; 25.
- Kristensen MS, Green A, Nybo M, Hede SM, Mikkelsen KH, Gislason G, Larsen ML, Ersbøll AK. Lipid-lowering therapy and low-density lipoprotein cholesterol goal attainment after acute coronary syndrome: a Danish population-based cohort study. BMC Cardiovasc Disord. 2020 Jul 13;20(1):336.
- Ray KK, Haq I, Bilitou A, Manu MC, Burden A, Aguiar C, Arca M, Connolly DL, Eriksson M, Ferrières J, Laufs U, Mostaza JM, Nanchen D, Rietzschel E, Strandberg T, Toplak H, Visseren FLJ, Catapano AL; SANTORINI Study Investigators. Treatment gaps in the implementation of LDL cholesterol control among high- and very high-risk patients in Europe between 2020 and 2021: the multinational observational SANTORINI study. Lancet Reg Health Eur. 2023; 29: 100624.
- De Luca L, Arca M, Temporelli PL, Meessen J, Riccio C, Bonomo P, Colavita AR, Gabrielli D, Gulizia MM, Colivicchi F; START Investigators. Current lipid lowering treatment and attainment of LDL targets recommended by ESC/EAS guidelines in very high-risk patients with established atherosclerotic cardiovascular disease: Insights from the START registry. Int J Cardiol. 2020 Oct 1;316:229-235.
- Colivicchi F. L’evoluzione del trattamento dell’ipercolesterolemia. G Ital Cardiol 2021; 22(4 Suppl.1):4S.
- Adams SP, Sekhon SS, Wright JM. Lipidlowering efficacy of rosuvastatin. Cochrane Database Syst Rev 2014; 11: CD010254.
- Toth PP, Dayspring TD. Drug safetyevaluation of rosuvastatin. Expert Opin DrugSaf 2011; 10: 969-86.
- Morrone D, Weintraub WS, Toth PP, Hanson ME, Lowe RS, Lin J, Shah AK, Tershakovec AM. Lipid-altering efficacy of ezetimibe plus statin and statin monotherapy and identification of factors associated with treatment response: a pooled analysis of over 21,000 subjects from 27 clinical trials. Atherosclerosis. 2012 Aug;223(2):251-61.
- Lee CW, Kang SJ, Ahn JM, Song HG, Lee JY, Kim WJ,Park DW, Lee SW, Kim YH, Park SW, Park SJ. Comparisonof effects of atorvastatin (20 mg) versus rosuvastatin (10mg) therapy on mild coronary atherosclerotic plaques (from the ARTMAP trial). Am J Cardiol. 2012 Jun15;109: 1700.
- Lablanche JM, Leone A, Merkely B, Morais J, Alonso J, Santini M, Eha J, Demil N, Licour M, Tardif JC; CENTAURUS investigators. Comparison of the efficacy of rosuvastatin versus atorvastatin in reducing apolipoprotein B/apolipoprotein A-1 ratio in patients with acute coronary syndrome: results of the CENTAURUS study. Arch Cardiovasc Dis. 2010; 103: 160-9.
- Ray KK, Molemans B, Schoonen WM, Giovas P, Bray S, Kiru G, Murphy J, Banach M, De Servi S, Gaita D, Gouni-Berthold I, Hovingh GK, Jozwiak JJ, Jukema JW, Kiss RG, Kownator S, Iversen HK, Maher V, Masana L, Parkhomenko A, Peeters A, Clifford P, Raslova K, Siostrzonek P, Romeo S, Tousoulis D, Vlachopoulos C, Vrablik M, Catapano AL, Poulter NR; DA VINCI study. EU-Wide Cross-Sectional Observational Study of Lipid-Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol. 2021 Sep 20;28(11):1279-1289.
- Di Fusco SA, Aquilani S, Spinelli A, Alonzo A, Matteucci A, Castello L, Imperoli G, Colivicchi F. The polypill strategy in cardiovascular disease prevention: It’s time for its implementation. Prog Cardiovasc Dis. 2023 Jul-Aug;79:37-40.
- De Cates AN, Farr MR, Wright N, et al. Fixed-Dose Combination Therapy for the Prevention of Cardiovascular Disease. Cochrane Database Syst Rev 2014;4:CD009868.
- Rea F, Savare L, Corrao G, Mancia G. Adherence to Lipid-Lowering Treatment by Single-Pill Combination of Statin and Ezetimibe. Adv Ther 2021; 38: 5270-85.
- Caldeira D, Vaz-Carneiro A, Costa J. The impact of dosing frequency on medication adherence in chronic cardiovascular disease: systematic review and metaanalysis. Rev Port Cardiol 2014; 33: 431-7.
- Bays HE, Davidson MH, Massaad R, Flaim D, Lowe RS, Tershakovec AM, Jones-Burton C. Safety and efficacy of ezetimibe added on to rosuvastatin 5 or 10 mg versus up-titration of rosuvastatin in patients with hypercholesterolemia (the ACTE Study). Am J Cardiol. 2011 Aug 15;108(4):523-30.
- Hong SJ, Jeong HS, Ahn JC, Cha DH, Won KH, Kim W, Cho SK, Kim SY, Yoo BS, Sung KC, Rha SW, Shin JH, Han KR, Chung WS, Hyon MS, Lee HC, Bae JH, Rhee MY, Kwan J, Jeon DW, Yoo KD, Kim HS. A Phase III, Multicenter, Randomized, Double-blind, Active Comparator Clinical Trial to Compare the Efficacy and Safety of Combination Therapy With Ezetimibe and Rosuvastatin Versus Rosuvastatin Monotherapy in Patients With Hypercholesterolemia: I-ROSETTE (Ildong Rosuvastatin & Ezetimibe for Hypercholesterolemia) Randomized Controlled Trial. Clin Ther. 2018 Feb;40(2):226-241.e4.
Introduzione
Malgrado la riduzione dell’incidenza e prevalenza delle coronaropatie negli ultimi 30 anni in tutti i paesi industrializzati dell’occidente, la patologia cardiovascolare rimane la causa principale di mortalità e di invalidità. Il progressivo invecchiamento della popolazione, il costante aumento del diabete e di alcuni fattori di rischio quali l’obesità e l’ipertensione arteriosa, aumenteranno ulteriormente l’incidenza, la prevalenza e il carico assistenziale ed economico legato alla patologia cardiovascolare, non solo nei paesi industrializzati ma anche nei paesi in via di sviluppo.
In Italia le malattie dell’apparato cardiovascolare sono la prima causa di morte nel complesso della popolazione e tra gli anziani, e la seconda tra gli adulti, subito dopo i tumori (1).
L’importanza della prevenzione cardiovascolare (CV) rimane indiscussa e deve essere promossa a diversi livelli, sia nella popolazione generale, attraverso la promozione di comportamenti e stili di vita sani sia a livello individuale soprattutto nei soggetti a medio ed alto rischio agendo sui fattori di rischio cardiovascolare, tra i quali i livelli lipidici, la pressione arteriosa e il diabete. Le nuove linee guida confermano che l’approccio al paziente parte dalla stratificazione in classi di rischio, a ciascuna delle quali viene assegnato un obiettivo terapeutico in termini di livelli di colesterolo LDL (C-LDL) secondo cui più basso è il livello di C-LDL, migliore è la prevenzione CV. In linea generale, i soggetti ad alto rischio dovrebbero essere identificati e gestiti prontamente. Le raccomandazioni indicano, per i pazienti a rischio molto alto (sia in prevenzione primaria che in quella secondaria), l’obiettivo di C-LDL <55 mg/dL (<1,4 mmol/L) e almeno il 50% di riduzione dei livelli basali. Nei pazienti ad alto rischio, l’obiettivo di C-LDL è <70 mg/dL (o <1,8 mmol/L) e almeno il 50% di riduzione dai livelli basali (Figura 1) (2, 3). La correlazione tra i livelli del colesterolo plasmatico e il rischio cardiovascolare è definita da una serie ormai ricca di studi osservazionali prospettici, condotti in varie aree del mondo; il nesso causale (e non semplicemente di associazione) tra questi due parametri è confermato dai risultati dei numerosi studi di intervento, randomizzati e controllati, che hanno documentato come la riduzione della colesterolemia stessa, ottenuta mediante interventi di varia natura (soprattutto di natura farmacologica), induca una proporzionale riduzione del rischio cardiovascolare e soprattutto coronarico. Questo complesso di evidenze, che si è andato accumulando nella letteratura scientifica, è stato integrato da una crescente attenzione alla caratterizzazione del paziente candidato all’intervento ipocolesterolemizzante, essenzialmente basata sulla stima del suo rischio cardiovascolare globale, e dalla definizione dell’ampiezza del calo dell’LDL o del valore obiettivo (target) da perseguire, mediante l’intervento terapeutico (3).
Un’efficace terapia farmacologica ipolipemizzante, quando la correzione degli stili di vita non risulti sufficiente, può prevenire lo sviluppo di coronaropatia e ridurre significativamente l’incidenza di eventi coronarici e cerebrovascolari.
L’avvento delle statine ha rivoluzionato la terapia farmacologica delle dislipidemie: numerosi trial clinici in prevenzione primaria e secondaria, nel soggetto ad alto rischio, nel paziente anziano, nel diabetico, nell’iperteso e nelle sindromi coronariche acute hanno documentato efficacia e sicurezza di questa classe farmacologica (4-6).
Ad oggi è possibile eseguire una gestione personalizzata del rischio cardiovascolare con idonei calcolatori. Ad esempio, il sito U-Prevent rappresenta un supporto alle decisioni cliniche certificato, attraverso l’inserimento dei dati clinici del paziente e dell’area geografia, per determinare un profilo di rischio individuale di sviluppare la malattia cardiovascolare e valutare le modifiche del rischio cardiovascolare ottenute con l’intervento terapeutico (7) (Figura 2).
Le Linee Guida
Le linee guida per la gestione della colesterolemia che si sono succedute negli ultimi vent’anni, hanno sottolineato come l’elemento che più si è modificato è l’obiettivo terapeutico degli interventi di controllo della colesterolemia. A partire dall’ormai storico documento denominato ATP-III, che nel 2001 suggeriva di portare la colesterolemia LDL dei soggetti in prevenzione secondaria, o portatori di “equivalenti coronarici” (arteriopatia obliterante degli arti inferiori, aneurisma dell’aorta addominale, malattia carotidea sintomatica), a un valore inferiore a 100 mg/dl, i documenti successivi, sia negli Stati Uniti sia in Europa, hanno indicato valori target progressivamente decrescenti. Nei soggetti con eventi recidivanti nonostante l’istituzione di un’efficace terapia ipocolesterolemizzante, l’obiettivo terapeutico per la colesterolemia LDL è ulteriormente ridotto a 40 mg/dl, quindi risulta ampliato il numero dei pazienti candidati a interventi più aggressivi su questo parametro, e la necessità di utilizzare più ampliamente farmaci a elevata efficacia (3).
Ruolo fondamentale è giocato anche dalla tempestività dell’inizio del trattamento. Diversi studi hanno dimostrato che l’adozione di una terapia ipolipemizzante intensiva entro 10 giorni da un episodio di SCA riduca il rischio in misura maggiore rispetto a regimi non intensivi. È raccomandabile iniziare sin dalla dimissione un trattamento con statina ad elevata intensità ed ezetimibe, in associazioni precostituite (8). La terapia ipolipemizzante deve continuare indefinitamente dopo la dimissione, avendo cura di verificare il raggiungimento e il mantenimento del target lipidico raccomandato nel tempo (C-LDL ridotto del 50% e <55mg/dl). Un primo controllo del C-LDL potrà essere effettuato dopo 4 settimane dalla dimissione, oppure secondo quanto previsto nei percorsi diagnostico-terapeutici assistenziali vigenti presso la singola struttura. Successivi controlli dovranno essere definiti in rapporto alle esigenze cliniche. In occasione di ogni controllo dovrà essere verificata l’aderenza del paziente alle prescrizioni e l’eventuale comparsa di effetti collaterali o reazioni avverse correlabili alla terapia ipolipemizzante.
A tal proposito, risulta importante non soltanto raggiungere i target terapeutici definiti a seconda dei profili di rischio e del grado di prevenzione, ma attuare un regime terapeutico il più intensivo possibile in modo tempestivo. Malgrado ciò numerosi pazienti in trattamento con questi farmaci non raggiungono di fatto il target terapeutico individuato dalle varie linee guida.
Tuttavia, nonostante le raccomandazioni delle linee guida, i dati di “real world” continuano a porre in evidenza le difficoltà a raggiungere i target indicati (9). A tal proposito, lo studio SANTORINI è uno studio multinazionale, prospettico, osservazionale, che fino ad oggi ha arruolato più di 9.500 pazienti da più di 800 centri in 14 Paesi in tutta Europa. I primi risultati mostrano che, al basale, il 18,6% dei pazienti a rischio cardiovascolare alto e molto alto non riceveva alcuna terapia ipolipemizzante (LLT). La maggior parte dei pazienti (54,1%) ha ricevuto LLT in monoterapia, e le terapie di associazione sono state utilizzate solo nel 27,3% dei pazienti. Esso dimostra e conferma la necessità di rivalutare e ripensare gli approcci per gestire i livelli di colesterolo nei pazienti ad alto e altissimo rischio di malattie cardiovascolari, assicurando in particolare che questi pazienti ricevano le terapie ipolipemizzanti più appropriate per tipo e dosaggio (10).
L’analisi dei dati dello studio START (in inglese STable Coronary Artery Diseases RegisTry) mostra un raggiungimento subottimale dei valori target di C-LDL nei pazienti a rischio cardiovascolare molto alto: valori di C-LDL <70 mg/dl sono ottenuti solo nel 58,1% dei pazienti, mentre solo il 3,2% raggiunge concentrazioni sieriche <55 mg/dl (11). Questo risultato sembra essere correlato anche ai potenziali eventi avversi legati alle statine (mialgie, dolori articolari, astenia, ecc.) che possono manifestarsi in 50-100 casi ogni 10.000 pazienti trattati per 5 anni. Ne consegue un sottoutilizzo dei farmaci ipolipemizzanti in pazienti ad alto rischio, con gravi ripercussioni sulla sopravvivenza e la qualità di vita degli stessi (12).
Le cause di questo gap tra target previsto dalle linee guida e target concretamente raggiunto nel “mondo reale” derivano probabilmente da numerosi fattori, quali ad esempio una terapia incongrua per dosaggio e continuità di somministrazione, una spesso ingiustificata paura di effetti collaterali, una inadeguata compliance da parte dei pazienti, ma anche dall’obiettiva difficoltà nel riuscire ad abbassare il colesterolo totale e LDL ai livelli consigliati dalle linee guida.
La terapia farmacologica delle dislipidemie
Le statine esercitano il loro effetto principale con la riduzione dei livelli di colesterolo LDL, inibendo competitivamente la HMG-CoA riduttasi e, di conseguenza, la sintesi endogena di colesterolo a livello epatico. La ridotta disponibilità di colesterolo cellulare determina un aumento dell’espressione sulla superficie degli epatociti del gene del recettore per le LDL che porta ad una aumentata rimozione delle LDL circolanti, riducendo così i livelli plasmatici del C-LDL.
La monoterapia con le statine è in genere ben tollerata, anche se con una frequenza non trascurabile si assiste alla comparsa di eventi avversi, i più importanti dei quali sono la miopatia e un aumento asintomatico delle transaminasi epatiche, nonché possibili interazioni con altri farmaci.
La rosuvastatina sembrerebbe rispondere positivamente alla maggior parte di questi requisiti, per la sua efficacia nel correggere simultaneamente le diverse alterazioni del profilo lipidico, per la sua efficacia di riduzione del C-LDL anche alle dosi più basse e quindi senza necessità di ulteriori adeguamenti, per i minimi rischi di interferenza con altri farmaci abitualmente utilizzati in associazione alle statine. Si tratta, in effetti, della molecola più efficace nel ridurre la colesterolemia tra le statine attualmente disponibili in Europa (13). La dose giornaliera varia da 5 a 40 mg. Dopo somministrazione per via orale la rosuvastatina viene ben assorbita dal tratto gastroenterico e la concentrazione plasmatica di picco viene raggiunta entro circa 5 ore dalla assunzione. La molecola è idrosolubile e presenta una biodisponibilità assoluta pari a circa il 20%. L’eliminazione avviene in forma immodificata nelle feci (90% circa), mentre la parte rimanente viene escreta nelle urine. L’emivita del farmaco è di circa 19 ore (14) consentendo l’eventuale assunzione ad inizio giornata.
Tuttavia, recenti evidenze, al fine di migliorare l’aderenza terapeutica grazie ad una riduzione degli effetti indesiderati secondari all’utilizzo di statina ad alta intensità, propongono di associare ad una statina ad intensità moderata l’ezetimibe. L’ezetimibe riduce significativamente la colesterolemia LDL anche in pazienti già in terapia con statina, essa porta ad un ulteriore e significativo beneficio clinico; inoltre, presenta altre azioni “antiaterosclerotiche” modulando il contenuto degli steroli vegetali e correggendo la disfunzione endoteliale.
Il diverso meccanismo d’azione di statine ed ezetimibe rende questi approcci terapeutici complementari nel ridurre i livelli di C-LDL e rappresenta il razionale per un loro impiego in associazione. Studi osservazionali hanno riportato che con l’uso delle statine in combinazione con ezetimibe i target terapeutici si ottengono con maggiore probabilità (rispettivamente il 21% e 58% dei pazienti raggiunge i valori raccomandati dalle ultime linee guida). Diverse evidenze hanno mostrato come, sia in termini di raggiungimento dei livelli target di C-LDL che di miglioramento di tutti i parametri lipidici considerati, sia più vantaggioso l’impiego della terapia di combinazione statina-ezetimibe, piuttosto che raddoppiare la dose iniziale di statina. Sulla base delle evidenze accumulate, le linee guida indicano la terapia di associazione come strategia terapeutica appropriata nei pazienti a rischio alto e molto alto che non raggiungono i target con la monoterapia. La combinazione della statina alla massima dose tollerata con l’ezetimibe viene indicata come prima opzione terapeutica, in particolare, nei pazienti a rischio molto elevato, così come quelli a rischio estremamente elevato (1 o più eventi entro 2 anni), potrebbe essere vantaggioso iniziare la terapia ipolipemizzante direttamente con la combinazione statine ed ezetimibe. Va anche rilevato che i meccanismi d’azione complementari di rosuvastatina e di ezetimibe, attivi, la prima sulla sintesi epatica del colesterolo e il secondo sul suo assorbimento intestinale, consentono di ottenere una risposta terapeutica, nei singoli individui, molto omogenea.
L’aggiunta di ezetimibe, al dosaggio standard di 10 mg/die, a una statina induce un calo aggiuntivo della colesterolemia dell’ordine del 18-20%, con un effetto complessivo sulla colesterolemia LDL pari a quello ottenibile se il dosaggio della statina venisse aumentato di otto volte, secondo la ben nota “regola del 6%”, senza indurre l’aumento del rischio di effetti collaterali (15) (Figura 3). Studi che hanno esaminato l’efficacia di rosuvastatina versus atorvastatina hanno evidenziato come la rosuvastatina sia più efficace nella rapida stabilizzazione della placca e di una maggiore regressione del suo volume (16) a fronte anche di un miglior rapporto apoB/ApoA1 lipoproteina (17).
La terapia di combinazione
Le osservazioni del mondo reale, tuttavia, attestano l’ampio divario circa l’effettivo conseguimento dei target raccomandati dalle linee guida. Nello studio osservazionale europeo DA VINCI solo il 18% dei 2.888 pazienti in prevenzione secondaria presentava un valore di C-LDL <55 mg/dl, di questi solo il 9% era in trattamento con statina a moderata/alta intensità + ezetimibe e il 45,8% era in trattamento con una statina a bassa o media intensità (18).
Questo potrebbe essere spiegato in parte dallo scarso impiego di terapie di combinazione, in parte dalla bassa aderenza al trattamento, ascrivibile, tra i diversi fattori, alla terapia poli-farmacologica stessa che impone al paziente con multiple comorbilità l’assunzione di diversi farmaci. La polipillola, contenente diversi agenti farmacologici mirati al controllo di uno o più fattori di rischio o di malattia, rappresenta una strategia di semplificazione della terapia che consente di favorire l’aderenza e migliorare gli outcomes clinici cardiovascolari (19).
Una revisione sistematica della letteratura, che ha incluso nove studi clinici randomizzati, ha evidenziato che una polipillola contenente almeno un agente antipertensivo e uno ipocolesterolemizzante è associata ad un’aderenza terapeutica del 33% superiore rispetto alla terapia standard (20). Ad oggi, le linee guida della Societa Europea di Cardiologia sulla gestione delle dislipidemie raccomandano l’impiego di farmaci che contengono più agenti terapeutici in un’unica compressa. Il peso della polifarmacologia sull’aderenza terapeutica è confermato anche dalla dimostrazione che i pazienti in terapia ipolipemizzante che ricevono l’associazione statina + ezetimibe in un’unica pillola presentano una probabilità dell’87% più elevata di essere altamente aderenti al trattamento rispetto a quelli che assumono i due farmaci separatamente, indipendentemente da età, genere o profilo clinico, e con una riduzione degli outcomes cardiovascolari del 55% rispetto ai pazienti con bassa aderenza (21).
Aggiungere ezetimibe ad una statina a dose fissa in una singola pillola aumenta l’aderenza terapeutica. La vera o presunta intolleranza e le non infrequenti riferite mialgie nei pazienti in terapia con statine, specialmente se lipofile e ad alte dosi, influenza grandemente l’aderenza terapeutica con conseguenze anche gravi sulla prognosi. L’adesione terapeutica risulta essere, probabilmente, la sfida più moderna e difficile per il medico e un primo passo concreto potrebbe essere quello di “semplificare” il più possibile la prescrizione terapeutica, utilizzando le combinazioni farmacologiche.
In conclusione, tali osservazioni suggeriscono che la terapia di associazione a dosi fisse e in una singola pillola determini non solo un più efficiente controllo dei livelli di C-LDL ed un possibile miglioramento degli outcomes con una significativa riduzione degli effetti collaterali, ma soprattutto un rilevante aumento dell’aderenza terapeutica, rinforzando sempre più in maniera convincente il potenziale ruolo della terapia di combinazione anche nella fase immediatamente post-acuta della sindrome coronarica acuta (SCA).
Terapie ipolipemizzanti e aderenza
Tra le diverse azioni implementate per migliorare l’aderenza, quelle che si sono rivelate maggiormente costo-efficaci e dunque in grado di incidere in maniera significativa sulla riduzione dei costi sanitari, sono rappresentate dagli interventi educativi rivolti ai pazienti e al personale sanitario, l’utilizzo di farmaci in associazione fissa o di polipillole che consentono di semplificare la terapia, il coinvolgimento delle farmacie e del personale sanitario, la riduzione della spesa out-of-pocket e il monitoraggio dell’aderenza tramite interventi ad hoc.
Indiscutibilmente la semplificazione degli schemi terapeutici rappresenta uno degli interventi più efficaci per migliorare l’aderenza terapeutica. Il frazionamento delle dosi di farmaco e la complessità dello schema terapeutico, infatti, impattano negativamente sull’aderenza (22).
Non sorprende, quindi, l’interesse che la letteratura scientifica ha rivolto nel corso degli anni all’uso in prevenzione cardiovascolare di combinazioni precostituite di farmaci, della stessa classe o di classi diverse, che consentissero da un lato di semplificare gli schemi terapeutici attraverso la riduzione del numero di compresse e dall’altro di massimizzare la resa preventiva sfruttando le sinergie farmacologiche. Le sinergie terapeutiche rappresentano senza dubbio uno strumento prezioso per il clinico in quanto consentono di raggiungere target terapeutici ambiziosi utilizzando combinazioni razionali di farmaci.
Conclusioni
Quando è presente ipercolesterolemia, dobbiamo porci alcune domande: chi è il paziente? Qual è il suo rischio cardiovascolare globale? Qual è il suo target di C-LDL? Quale terapia farmacologica? Alla luce di questi quesiti, occorre conoscere prima di tutto la storia clinica personale e familiare del paziente, i suoi dati ematochimici e il suo profilo lipidico.
Le più recenti linee guida internazionali, sulla base dei risultati degli studi di osservazione e di intervento disponibili in letteratura, propongono obiettivi terapeutici molto ambiziosi, in linea con la filosofia “the lower, the better”. Ne discende l’esigenza di ridurre spesso in maniera molto marcata la colesterolemia LDL, soprattutto nei pazienti ad alto o altissimo rischio. La disponibilità di una combinazione a dosaggio fisso tra rosuvastatina ed ezetimibe consente di affrontare e risolvere, in un numero significativo di pazienti, il problema della riduzione della colesterolemia LDL. Sono soprattutto importanti, al proposito, l’ampio effetto sulla colesterolemia LDL, l’elevata tollerabilità (soprattutto in termini di basso rischio di interazioni farmacologiche), l’elevata prevedibilità della risposta terapeutica a questa combinazione, dovuta alla contemporanea presenza di molecole con effetti sulla sintesi ma anche sull’assorbimento del colesterolo, e – non ultimo – il costo contenuto.
Le più recenti evidenze scientifiche enfatizzano l’efficacia della polipillola nella prevenzione cardiovascolare, integrando con successo il concetto di semplificazione terapeutica con una sinergia di efficacia protettiva. Questo approccio moderno rappresenta un tassello imprescindibile per la gestione ottimale del paziente cardiovascolare.
Bibliografia
- Clinical trials with rosuvastatin: efficacy and safety of its use Schweiger C. Ital Heart J. 2003 Dec;4 Suppl 7:33S-46S.
- Cholesterol Treatment Trialists’ – CTT – Collaboration. Efficacy and safety of LDL-lowering therapy among men and women: meta-analysis of individual data from 174 000 participants in 27 randomised trials. Lancet 2015; 385:1397-405.
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188.
- Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 5963 people with diabetes: a randomised placebo controlled trial. Lancet 2003; 361: 2005-16.
- Sever PS, Dahlöf B, Poulter NR, Wedel H, Beevers G, Caulfield M, Collins R, Kjeldsen SE, Kristinsson A, McInnes GT, Mehlsen J, Nieminen M, O’Brien E, Ostergren J; ASCOT investigators. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial–Lipid Lowering Arm (ASCOT-LLA): a multicentre randomised controlled trial. Lancet. 2003 Apr 5;361(9364):1149-58.
- Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, Zeiher A, Chaitman BR, Leslie S, Stern T; Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) Study Investigators. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA. 2001 Apr 4;285(13):1711-8.
- U-Prevent site powered by ORTEC. Version: 293. https://u-prevent.com/
- De Luca L, Di Fusco SA, Iannopollo G, Mistrulli R, Rizzello V, Aimo A, Navazio A, Bilato C, Corda M, Di Marco M, Geraci G, Iacovoni A, Milli M, Pascale V, Riccio C, Scicchitano P, Tizzani E, Gabrielli D, Grimaldi M, Colivicchi F, Oliva F. Scientific statement ANMCO sulla semplificazione del regime terapeutico farmacologico in prevenzione secondaria. G Ital Cardiol 2024; 25.
- Kristensen MS, Green A, Nybo M, Hede SM, Mikkelsen KH, Gislason G, Larsen ML, Ersbøll AK. Lipid-lowering therapy and low-density lipoprotein cholesterol goal attainment after acute coronary syndrome: a Danish population-based cohort study. BMC Cardiovasc Disord. 2020 Jul 13;20(1):336.
- Ray KK, Haq I, Bilitou A, Manu MC, Burden A, Aguiar C, Arca M, Connolly DL, Eriksson M, Ferrières J, Laufs U, Mostaza JM, Nanchen D, Rietzschel E, Strandberg T, Toplak H, Visseren FLJ, Catapano AL; SANTORINI Study Investigators. Treatment gaps in the implementation of LDL cholesterol control among high- and very high-risk patients in Europe between 2020 and 2021: the multinational observational SANTORINI study. Lancet Reg Health Eur. 2023; 29: 100624.
- De Luca L, Arca M, Temporelli PL, Meessen J, Riccio C, Bonomo P, Colavita AR, Gabrielli D, Gulizia MM, Colivicchi F; START Investigators. Current lipid lowering treatment and attainment of LDL targets recommended by ESC/EAS guidelines in very high-risk patients with established atherosclerotic cardiovascular disease: Insights from the START registry. Int J Cardiol. 2020 Oct 1;316:229-235.
- Colivicchi F. L’evoluzione del trattamento dell’ipercolesterolemia. G Ital Cardiol 2021; 22(4 Suppl.1):4S.
- Adams SP, Sekhon SS, Wright JM. Lipidlowering efficacy of rosuvastatin. Cochrane Database Syst Rev 2014; 11: CD010254.
- Toth PP, Dayspring TD. Drug safetyevaluation of rosuvastatin. Expert Opin DrugSaf 2011; 10: 969-86.
- Morrone D, Weintraub WS, Toth PP, Hanson ME, Lowe RS, Lin J, Shah AK, Tershakovec AM. Lipid-altering efficacy of ezetimibe plus statin and statin monotherapy and identification of factors associated with treatment response: a pooled analysis of over 21,000 subjects from 27 clinical trials. Atherosclerosis. 2012 Aug;223(2):251-61.
- Lee CW, Kang SJ, Ahn JM, Song HG, Lee JY, Kim WJ,Park DW, Lee SW, Kim YH, Park SW, Park SJ. Comparisonof effects of atorvastatin (20 mg) versus rosuvastatin (10mg) therapy on mild coronary atherosclerotic plaques (from the ARTMAP trial). Am J Cardiol. 2012 Jun15;109: 1700.
- Lablanche JM, Leone A, Merkely B, Morais J, Alonso J, Santini M, Eha J, Demil N, Licour M, Tardif JC; CENTAURUS investigators. Comparison of the efficacy of rosuvastatin versus atorvastatin in reducing apolipoprotein B/apolipoprotein A-1 ratio in patients with acute coronary syndrome: results of the CENTAURUS study. Arch Cardiovasc Dis. 2010; 103: 160-9.
- Ray KK, Molemans B, Schoonen WM, Giovas P, Bray S, Kiru G, Murphy J, Banach M, De Servi S, Gaita D, Gouni-Berthold I, Hovingh GK, Jozwiak JJ, Jukema JW, Kiss RG, Kownator S, Iversen HK, Maher V, Masana L, Parkhomenko A, Peeters A, Clifford P, Raslova K, Siostrzonek P, Romeo S, Tousoulis D, Vlachopoulos C, Vrablik M, Catapano AL, Poulter NR; DA VINCI study. EU-Wide Cross-Sectional Observational Study of Lipid-Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol. 2021 Sep 20;28(11):1279-1289.
- Di Fusco SA, Aquilani S, Spinelli A, Alonzo A, Matteucci A, Castello L, Imperoli G, Colivicchi F. The polypill strategy in cardiovascular disease prevention: It’s time for its implementation. Prog Cardiovasc Dis. 2023 Jul-Aug;79:37-40.
- De Cates AN, Farr MR, Wright N, et al. Fixed-Dose Combination Therapy for the Prevention of Cardiovascular Disease. Cochrane Database Syst Rev 2014;4:CD009868.
- Rea F, Savare L, Corrao G, Mancia G. Adherence to Lipid-Lowering Treatment by Single-Pill Combination of Statin and Ezetimibe. Adv Ther 2021; 38: 5270-85.
- Caldeira D, Vaz-Carneiro A, Costa J. The impact of dosing frequency on medication adherence in chronic cardiovascular disease: systematic review and metaanalysis. Rev Port Cardiol 2014; 33: 431-7.
- Bays HE, Davidson MH, Massaad R, Flaim D, Lowe RS, Tershakovec AM, Jones-Burton C. Safety and efficacy of ezetimibe added on to rosuvastatin 5 or 10 mg versus up-titration of rosuvastatin in patients with hypercholesterolemia (the ACTE Study). Am J Cardiol. 2011 Aug 15;108(4):523-30.
- Hong SJ, Jeong HS, Ahn JC, Cha DH, Won KH, Kim W, Cho SK, Kim SY, Yoo BS, Sung KC, Rha SW, Shin JH, Han KR, Chung WS, Hyon MS, Lee HC, Bae JH, Rhee MY, Kwan J, Jeon DW, Yoo KD, Kim HS. A Phase III, Multicenter, Randomized, Double-blind, Active Comparator Clinical Trial to Compare the Efficacy and Safety of Combination Therapy With Ezetimibe and Rosuvastatin Versus Rosuvastatin Monotherapy in Patients With Hypercholesterolemia: I-ROSETTE (Ildong Rosuvastatin & Ezetimibe for Hypercholesterolemia) Randomized Controlled Trial. Clin Ther. 2018 Feb;40(2):226-241.e4.
Related papers
La pubblicazione recente di alcuni lavori scientifici basati sulle risultanze di alcuni osservatori epidemiologi mondiali, ha riportato alla ribalta il ruolo chiave delle malattie cardiovascolari come prima causa di morte e disabilità, non solo nel presente, ma anche nel futuro proiettato oggi al 2050 con un incremento più o meno equamente distribuito tra le malattie [more info]
1) Lipoproteine ed aterosclerosi Le lipoproteine sono particelle composte da un nucleo ricco in esteri del colesterolo e trigliceridi (TG) circondati da colesterolo libero, fosfolipidi e apolipoproteine. Le lipoproteine plasmatiche vengono suddivise in varie classi (VLDL, IDL, LDL, HDL e chilomicroni) in base alle dimensioni, alla composizione lipidica e alle apolipoproteine presenti (Tabella 1). I [more info]
Introduzione Le malattie cardiovascolari rappresentano la principale causa di morbilità e mortalità a livello globale, nonostante i progressi nella prevenzione e nel trattamento farmacologico. In questo contesto, l’adozione di strategie terapeutiche efficaci per la gestione dei fattori di rischio cardiovascolare è fondamentale. La combinazione farmacologica di farmaci con meccanismi d’azione complementari è diventata una pratica [more info]