- Ipertensione: stato dell’arte
Uno studio dell’Imperial College di Londra, pubblicato su The Lancet nel 2021, afferma che il numero di adulti tra i 30 e i 79 anni affetti da ipertensione a livello globale è aumentato da 650 milioni a 1,28 miliardi negli ultimi trent’anni (1). L’ipertensione è un importante fattore di rischio modificabile, che aumenta significativamente la possibilità di sviluppare complicanze cardiovascolari, cerebrovascolari e renali (2,3). Ciononostante, sono oltre 700 milioni i soggetti ipertesi a non ricevere trattamento (4) e, tra quelli trattati, solo il 20-30% raggiunge i valori raccomandati di pressione sanguigna (2). L’ipertensione incontrollata è persistentemente responsabile della maggioranza delle malattie cardiovascolari tra cui infarto miocardico, ictus ischemico e insufficienza cardiaca congestizia, determinando così un elevato numero di decessi per cause cardiovascolari in vari Paesi, inclusa l’Italia (2,5). Le linee guida ESC/ESH hanno fissato, come valori soglia oltre cui si è definiti ipertesi, 140 mmHg per la pressione sistolica e 90 mmHg per la pressione diastolica (6). Il raggiungimento di valori al di sotto di questa soglia è raccomandato indipendentemente da genere d’appartenenza, età, etnia o condizione clinica concomitante (2).
Seguire una terapia antipertensiva previene morbilità e mortalità cardiovascolare ed è compito del clinico spronare il paziente affinché quest’ultimo aderisca al trattamento assegnatogli, incentivandolo inoltre a modificare il suo stile di vita e a prendersi cura delle condizioni di comorbilità che possono peggiorarne la salute complessiva e la qualità della vita. Circa la metà degli individui in terapia antipertensiva interrompe spontaneamente il farmaco prescritto, indipendentemente dal raggiungimento dei livelli pressori raccomandati, spesso anche a causa di una mancata tollerabilità nei confronti del farmaco assegnato (5). Scegliere il giusto farmaco per ogni paziente è infatti fondamentale e il clinico deve dunque conoscere e selezionare la terapia più adatta ad ogni situazione e caso clinico. Non solo esistono svariate classi di farmaci antipertensivi, con meccanismi d’azione ben distinti, ma vi è anche un’ampia scelta di composti all’interno di ciascuna di queste classi, e le specifiche proprietà di ciascuno di questi può determinare un diverso esito clinico. Tra gli agenti antipertensivi raccomandati in prima linea per il trattamento dell’ipertensione troviamo: gli inibitori dell’enzima di conversione dell’angiotensina (noti come ACE-inibitori), gli antagonisti del recettore dell’angiotensina (noti come sartani o ARBs, Angiotensin Receptor Blockers), i beta-bloccanti, i diuretici e, infine, i calcio-antagonisti, oggetto di approfondimento in questo numero di PCR.
- Farmaci calcio-antagonisti
I calcio-antagonisti sono tra i farmaci raccomandati in prima linea per il trattamento dell’ipertensione e delle comorbidità correlate, e sono ideali sia per l’utilizzo in monoterapia che in doppia o tripla combinazione con altri agenti antipertensivi (2). Essi agiscono sui canali voltaggio-dipendenti di tipo L degli ioni calcio – dove “L” sta per “long-lasting”, riferendosi alla durata dell’attivazione del canale – posizionati sulla membrana di cellule della muscolatura liscia dei vasi sanguigni e di cellule cardiache. Se stimolati, questi canali si aprono permettendo l’afflusso degli ioni calcio all’interno della cellula (depolarizzazione) e innescando la contrazione delle fibre di actina e miosina. I calcio-antagonisti (o bloccanti dei canali del calcio) bloccano, per l’appunto, l’apertura del canale inibendo lo stimolo alla contrazione. La scoperta di questa classe di farmaci è scaturita da uno studio farmacologico degli anni ’60 che valutava varie molecole per la dilatazione coronarica (7). I calcio-antagonisti agiscono rilassando le cellule muscolari lisce dei vasi sanguigni, favorendo la vasodilatazione, riducendo la resistenza vascolare e, perciò, riducendo la pressione sanguigna (8). Tale azione vasodilatatoria può inoltre favorire la natriuresi attraverso l’aumento del flusso sanguigno a livello renale, la dilatazione delle arteriole afferenti e l’aumento della pressione di filtrazione glomerulare (8–10). Vi sono oltretutto evidenze che i calcio-antagonisti interferiscano con l’attività a-adrenergica che regola la contrattilità della muscolatura liscia, meccanismo che potrebbe ulteriormente contribuire all’effetto vasodilatatorio di questa classe di farmaci (9,11,12).
I calcio-antagonisti sono una classe eterogenea, ne esistono infatti tre gruppi definiti dall’affinità ai canali del calcio vascolari e cardiaci. La classe attualmente più comune è quella degli agenti diidropiridinici, che agiscono prevalentemente come dilatatori dei vasi periferici; le altre due classi sono i fenilalchilaminici, attivi a livello cardiaco, e i benzotiazepinici, che hanno un profilo d’affinità intermedio (5). Nel corso degli anni, molti studi clinici hanno dimostrato la capacità dei calcio-antagonisti di ridurre mortalità e morbilità cardiovascolare (2). Lo studio Syst-Eur (Systolic Hypertension in Europe), ideato per valutare i benefici cardiovascolari dell’impiego di un calcio-antagonista appartenente al gruppo delle diidropiridine, è stato interrotto dopo circa 2 anni per l’evidente riduzione del tasso di complicanze cardiovascolari nel gruppo assegnato al trattamento attivo rispetto al placebo (13). Lo studio FEVER (Felodipine EVEnt Reduction) ha anch’esso dimostrato la sostanziale riduzione di eventi cardiovascolari gravi e di mortalità nei pazienti in trattamento con un altro calcio-antagonista diidropiridinico, rispetto al placebo (14). Nel confronto, invece, tra calcio-antagonisti e altri agenti antipertensivi, svariati studi hanno attestato la validità del beneficio di protezione cardiovascolare conseguente all’impiego di farmaci calcio-antagonisti. È il caso, ad esempio, degli studi STOP Hypertension-2 (Swedish Trial in Old Patients with Hypertension-2 Study), INSIGHT (International Nifedipine GITS Study: Intervention as a Goal in Hypertension Treatment) e SHELL (Systolic Hypertension in the Elderly), che hanno riportato un’efficacia antipertensiva e di prevenzione da ictus equivalente ad alcuni farmaci comunemente impiegati nel trattamento dell’ipertensione (15–17). Alcuni di questi studi prevedevano inoltre terapie combinate con più agenti antipertensivi, al fine di valutare le combinazioni più efficaci a questo scopo. In sintesi, i calcio-antagonisti hanno comprovate evidenze di riduzione di morbilità e di mortalità cardiovascolare, sia in monoterapia che in combinazione ad altri agenti antipertensivi, e sono per questo raccomandati per il trattamento dell’ipertensione dalle linee guida ESC/ESH (2,6). Insieme ai farmaci inibitori del sistema renina-angiotensina, i calcio-antagonisti sono attualmente tra le strategie antipertensive più efficaci e meglio tollerate rispetto ad altre classi di farmaci (2). Come raccomandato dalle linee guida ESC/ESH, nei pazienti che non raggiungono i valori pressori target in monoterapia, calcio-antagonisti e farmaci inibitori del sistema renina-angiotensina possono essere combinati al fine di ottenere un miglior controllo pressorio (6). In questo contesto, le due classi di farmaci esistono anche in singole formulazioni a combinazione fissa al fine di favorire l’aderenza alla terapia. Nei casi in cui anche il duplice approccio non dovesse rivelarsi sufficientemente efficace, è possibile passare a una triplice terapia che coniuga calcio-antagonisti, inibitori del sistema renina-angiotensina e diuretici, al fine di massimizzare l’azione sinergica per raggiungere l’efficacia antipertensiva attraverso molteplici meccanismi d’azione (6).
- Barnidipina
3.1. Indicazioni e posologia
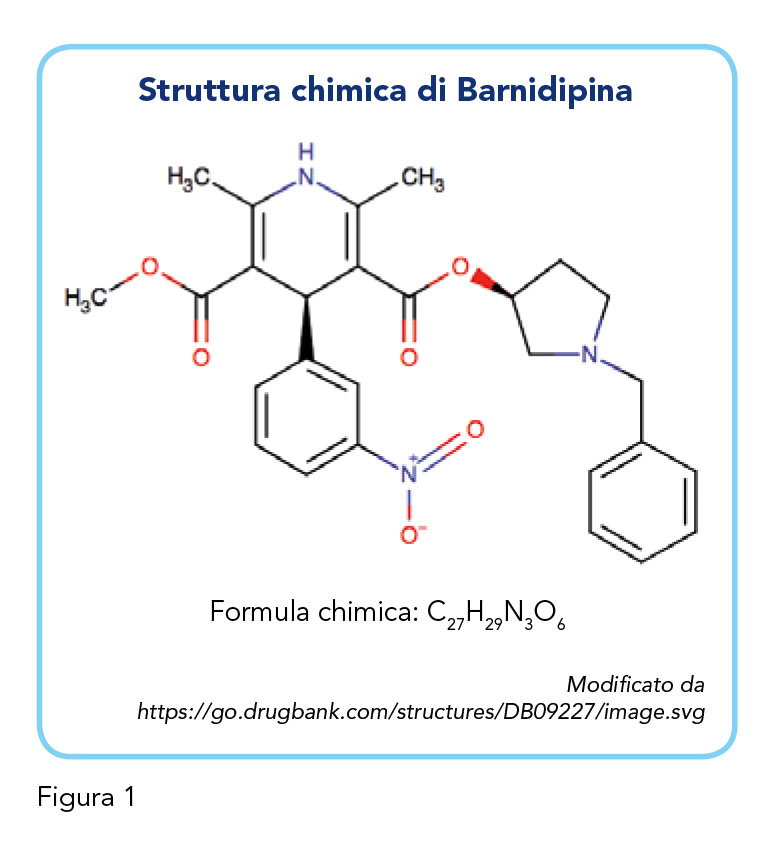
Barnidipina è un calcio-antagonista diidropiridinico che, come altri membri di questa classe di farmaci, è selettivo per i canali del calcio di tipo L (ad azione prolungata) ed è composta da un singolo isomero ottico (configurazione S,S). La struttura molecolare di Barnidipina è mostrata nella Figura 1. Barnidipina produce il suo effetto antipertensivo bloccando selettivamente l’afflusso di ioni calcio attraverso i canali “voltaggio-dipendenti” di tipo L nelle membrane eccitabili delle cellule muscolari lisce vascolari, come risultato dell’interazione con specifici recettori dei canali del calcio di tipo L, provocando vasodilatazione e conseguente riduzione delle resistenze periferiche (18-20). Barnidipina è disponibile in una formulazione a rilascio modificato per somministrazione orale una volta al giorno nel trattamento di pazienti con ipertensione essenziale da lieve a moderata. Le capsule vanno assunte preferibilmente con un bicchiere d’acqua, prima, durante o dopo i pasti.
La dose iniziale di Barnidipina raccomandata in RCP è di 10 mg una volta al giorno al mattino, ma può essere aumentata a 20 mg una volta al giorno, se necessario. Tuttavia, la decisione di aumentare la dose deve essere presa solo dopo aver ottenuto una completa stabilità dei valori pressori con la dose iniziale, che di solito avviene dopo 3-6 settimane. Poiché non sono disponibili dati nei bambini (< 18 anni), Barnidipina non deve essere somministrata nella popolazione pediatrica. La dose non deve essere aggiustata in pazienti anziani, anche se in questa popolazione è raccomandata una maggiore attenzione all’inizio del trattamento. Nei pazienti con compromissione renale da lieve a moderata bisogna prestare attenzione quando si aumenta la dose da 10 a 20 mg una volta al giorno.
3.2. Meccanismo d’azione
Barnidipina è un calcio antagonista lipofilo diidropiridinico caratterizzato da una lenta insorgenza d’azione e da un legame forte e duraturo con i canali del calcio di tipo L. Barnidipina mostra un’elevata affinità per i canali espressi nelle cellule muscolari lisce della parete vascolare, per cui il suo principale meccanismo d’azione deriva dalla riduzione della resistenza vascolare periferica secondaria alla sua azione vasodilatatoria. L’afflusso di ioni calcio attraverso canali “voltaggio-dipendenti” di tipo L nelle membrane eccitabili delle cellule muscolari lisce promuove la formazione di ponti incrociati calcio-dipendenti tra miosina e actina, le due principali proteine contrattili che guidano la contrazione. Bloccando i canali del calcio di tipo L “voltaggio-dipendenti”, Barnidipina blocca selettivamente l’afflusso di ioni calcio nelle cellule muscolari lisce e inibisce l’attivazione delle proteine contrattili (21,22). Come altri calcio-antagonisti diidropiridinici, si ipotizza che Barnidipina interagisca con la subunità alfa 1-C dei canali del calcio di tipo L, e che la subunità alfa 1-C del canale risieda all’interno del poro a doppio strato o del poro del canale, in una posizione più vicina alla superficie extracellulare che a quella intracellulare della membrana. Si ritiene che la lipofilia sia la probabile ragione di questa interazione e il motivo probabile per cui Barnidipina mostra un inizio lento e una lunga durata d’azione. Essendo una molecola altamente lipofila con un coefficiente di ripartizione ottanolo/acqua pari a 2.000, ci si aspetta che Barnidipina si accumuli nella membrana cellulare e, di conseguenza, acceda al suo recettore bersaglio in modo lento (21,22).
3.3. Farmacocinetica
Barnidipina è prontamente assorbita dal tratto gastrointestinale, ma subisce un esteso metabolismo di primo passaggio. La biodisponibilità assoluta della formulazione a rilascio modificato di Barnidipina valutata dopo una singola infusione di 6 ore da 0,75 mg e dopo una singola dose orale da 20 mg in volontari sani è stata dell’1,1%. La biodisponibilità della formulazione a rilascio modificato di Barnidipina, inoltre, non è influenzata in modo significativo dall’assunzione di cibo in volontari sani, né la farmacocinetica di questa formulazione è influenzata dall’età, dal sesso o dalla funzione renale (18). Il legame in vitro di Barnidipina con le proteine plasmatiche, principalmente con l’albumina, è compreso tra il 92,4% e il 98,9%. I test di legame con le proteine non hanno mostrato interazioni con farmaci quali amitriptilina, diazepam, diclofenac, fenitoina e warfarin. L’area sotto la curva della concentrazione plasmatica (AUC) ottenuta con la formulazione a rilascio modificato (2,85 μg/L∙h) è pari al 97% di quella ottenuta con la formulazione convenzionale in uno studio crossover condotto su volontari sani. La concentrazione plasmatica di picco di Barnidipina dopo una singola dose da 10 mg della formulazione a rilascio modificato è stata di 0,48 μg/L∙h. Dopo la somministrazione di singole dosi orali di Barnidipina radiomarcata nei ratti, i livelli di radioattività sono risultati più elevati nel rene, nel fegato e nel tratto gastrointestinale rispetto al plasma, mentre il cervello ha mostrato il livello più basso di radioattività (1).
3.4. Sicurezza e tollerabilità
Barnidipina è controindicata in caso di: ipersensibilità al principio attivo (o a una qualsiasi altra diidropiridina) o a uno qualsiasi degli eccipienti; grave compromissione renale (clearance della creatinina < 10 mL/min); angina pectoris instabile e infarto miocardico acuto (nelle prime 4 settimane); insufficienza cardiaca non in trattamento. I livelli ematici di Barnidipina possono aumentare quando viene usata in associazione con potenti inibitori del CYP3A4 (come risulta da studi di interazione in vitro), motivo per cui non va usata in associazione ad antiproteasici, ketoconazolo, itraconazolo, eritromicina e claritromicina. Si consiglia cautela nell’uso concomitante di deboli inibitori o induttori del CYP3A4. In caso di uso concomitante con inibitori del CYP3A4 si sconsiglia di aumentare il dosaggio di Barnidipina a 20 mg. Si consiglia inoltre cautela nell’uso concomitante di Barnidipina e cimetidina.
La contemporanea somministrazione di Barnidipina e di altri antipertensivi può determinare un effetto antipertensivo addizionale. Barnidipina può essere impiegato in concomitanza con beta-bloccanti o ACE-inibitori. Altre possibili interazioni farmacologiche potrebbero non essere note per mancanza di studi dedicati.
Barnidipina deve essere impiegato con cautela in pazienti con compromissione renale da lieve a moderata (clearance della creatinina compresa fra 10 e 80 mL/min). L’associazione di un calcio-antagonista con un farmaco che esercita un effetto inotropo negativo può provocare scompenso cardiaco, ipotensione o un (altro) infarto miocardico in pazienti ad alto rischio (ad es. pazienti con anamnesi di infarto miocardico). Come per tutti i derivati diidropiridinici, anche Barnidipina va usato con cautela in pazienti con disfunzione ventricolare sinistra, in pazienti con ostruzione del canale di efflusso del ventricolo sinistro e in pazienti con scompenso isolato del cuore destro. Barnidipina non è stata studiata in pazienti di classe III o IV della New York Heart Association Functional Classification (NYHA). È raccomandata cautela anche quando Barnidipina viene somministrata a pazienti con malattia del nodo del seno (in assenza di pacemaker).
Una dose più elevata di Barnidipina può essere necessaria quando viene somministrata in concomitanza con farmaci induttori enzimatici, come fenitoina, carbamazepina e rifampicina. Qualora il paziente dovesse smettere di usare un farmaco induttore enzimatico, si deve prendere in considerazione la riduzione della dose di Barnidipina. In base ai risultati di studi di interazione in vitro con (fra gli altri) simvastatina, metoprololo, diazepam e terfenadina, si ritiene improbabile che Barnidipina abbia effetti sulla farmacocinetica di altri farmaci che vengono metabolizzati dagli isoenzimi del citocromo P450.
Uno studio di interazione in vivo ha dimostrato che Barnidipina non influenza la farmacocinetica della digossina. In uno studio di interazione, l’alcool ha determinato un aumento dei livelli plasmatici di Barnidipina (40%), che non viene considerato clinicamente rilevante. Come con tutti i vasodilatatori e gli antipertensivi, si deve prestare cautela nell’assunzione concomitante di alcool poiché esso potrebbe potenziarne gli effetti. Nonostante la cinetica di Barnidipina non sia stata modificata significativamente dalla somministrazione di succo di pompelmo, è stato osservato un modico effetto.
Non esistono dati clinici sull’uso di Barnidipina in gravidanza o durante l’allattamento e studi sugli animali non suggeriscono effetti dannosi diretti, ma solo indiretti, sulla gravidanza né sullo sviluppo dell’embrio/fetale o postnatale. La classe delle diidropiridine ha mostrato la potenzialità di prolungare il travaglio e il parto, che non sono stati osservati con Barnidipina. Pertanto Barnidipina può essere usata in gravidanza solo se il beneficio giustifica il rischio potenziale per il feto. Studi sugli animali hanno inoltre dimostrato che Barnidipina (o i suoi metaboliti) viene escreto nel latte umano, motivo per il quale l’allattamento al seno non è consigliato durante l’uso di questo farmaco. Non sono stati effettuati studi sugli effetti di Barnidipina sulla capacità di guidare veicoli e di utilizzare macchinari, ma si consiglia comunque cautela, in quanto capogiri o vertigini possono presentarsi durante un trattamento antipertensivo.
Tra gli effetti indesiderati noti (da comuni a molto comuni in base al dosaggio) si annoverano cefalea, capogiri/vertigini, palpitazioni, vampate di calore ed edema periferico. I sintomi tendono a diminuire o a scomparire durante il trattamento (entro 1 mese l’edema periferico ed entro 2 settimane le vampate di calore, la cefalea e le palpitazioni). Sebbene non sia stata mai osservata, l’iperplasia gengivale può essere rilevante come avviene con l’impiego di altre diidropiridine. Alcune diidropiridine possono raramente causare dolore precordiale ed angina pectoris. Molto raramente pazienti con preesistente angina pectoris potrebbero osservare aumentata frequenza, durata e gravità di tali attacchi. Potrebbero osservarsi casi isolati di infarto miocardico.
I sintomi clinici dopo un sovradosaggio di calcio-antagonisti si sviluppano entro 30-60 minuti dopo la somministrazione di una dose da 5 a 10 volte superiore alla dose terapeutica. Possono essere teoricamente previsti i seguenti effetti collaterali: ipotensione, effetti elettrofisiologici (bradicardia sinusale, prolungamento della conduzione AV, blocco AV di II e III grado, tachicardia), effetti sul sistema nervoso centrale (sonnolenza, confusione e, raramente, convulsioni), sintomi gastrointestinali (nausea e vomito) ed effetti metabolici (iperglicemia). Il trattamento ospedaliero è necessario nell’eventualità di un’intossicazione. Sono indicati il trattamento sintomatico e il monitoraggio continuo dell’ECG. Nell’eventualità di un sovradosaggio, la lavanda gastrica deve essere eseguita il più presto possibile. Deve essere praticata un’iniezione endovenosa (alla dose di 0,2 mL/kg di peso corporeo) di calcio (preferibilmente 10 mL di una soluzione di cloruro di calcio al 10%) nel corso di 5 minuti, fino a una dose totale di 10 mL al 10%. La contrattilità del miocardio, il ritmo sinusale e la conduzione atrioventricolare verranno quindi migliorati. Il trattamento può essere ripetuto ogni 15-20 minuti (fino a un totale di 4 dosi) in base alla risposta del paziente, controllando i livelli di calcio.
3.5. Studi
- Sottoanalisi dello studio BASIC-HT (23): efficacia e tollerabilità di Barnidipina sono comparabili nei pazienti con ipertensione arteriosa giovani e anziani secondo dati di real-life
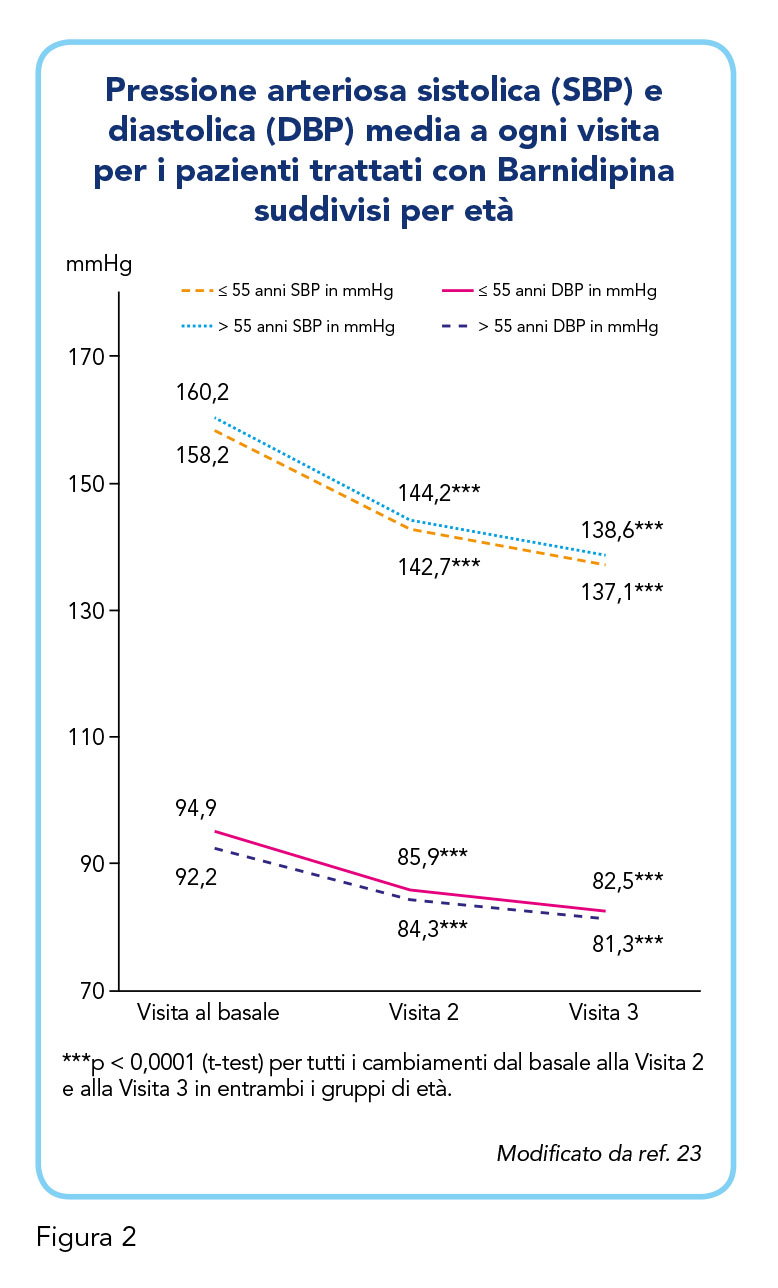
In generale, Barnidipina ha dimostrato di essere un farmaco antipertensivo efficace nella gestione dell’ipertensione essenziale nei pazienti anziani (18,24) senza subire l’influenza negativa dell’età (25). La sua tollerabilità è considerata generalmente molto buona nella maggior parte dei pazienti, compresi gli over 75 (18,24,25). La tollerabilità e l’efficacia di Barnidipina (10 mg o 20 mg) sono state studiate, nel 2015, in uno studio osservazionale prospettico su larga scala, open-label, in pazienti con ipertensione essenziale, compresi pazienti con concomitante diabete mellito (n=20.275) (BASIC-HT; BArnidipine real-life Safety and tolerability In Chronic HyperTension) (26). I risultati hanno confermato l’efficacia di Barnidipina nel contesto reale della pratica clinica di routine nella riduzione della pressione arteriosa: questo effetto sembrava inoltre essere dovuto alla buona aderenza alla terapia da parte dei pazienti. I risultati hanno anche mostrato il buon profilo di tollerabilità di Barnidipina (26). Due anni dopo, gli autori hanno pubblicato uno studio − analisi di sottogruppo per età pre-specificate nel protocollo − in cui descrivono l’efficacia e la tollerabilità del trattamento con Barnidipina, sia in monoterapia che in combinazione, in pazienti anziani rispetto a quelli più giovani. I dati relativi alla pressione arteriosa e alla frequenza cardiaca sono stati valutati nei sottogruppi di pazienti di età ≤ 55 anni rispetto a quelli di età > 55 anni: questo cut-off dell’età è di specifica importanza per l’obiettivo della pressione arteriosa e per la scelta del farmaco come trattamento di prima linea secondo le linee guida internazionali (27). In particolare, la maggior parte dei pazienti aveva un’età superiore ai 55 anni (n=14.023; 71,7%; età media: 69,3 anni), circa un quarto dei pazienti (n=4.778; 24,4%) aveva un’età compresa tra i 55 e i 64 anni, e circa la metà dei pazienti aveva un’età ≥ 65 anni (n=9.245; 47,3%): di questi ultimi, n=3.597 pazienti (18,4%) avevano più di 75 anni. La frequenza degli eventi avversi è stata ripartita in base alle fasce d’età dei pazienti < 65 anni e ≥ 65 anni perché questi ultimi hanno maggiori probabilità di sviluppare eventi avversi comuni a molti calcio-antagonisti, tra cui edema, ed eventi avversi cardiaci, come tachicardia e/o palpitazioni. Dai risultati al follow-up di 3 mesi è emersa una riduzione statisticamente significativa, e altrettanto clinicamente importante, della pressione arteriosa sistolica e della pressione arteriosa diastolica sia nei pazienti più giovani che in quelli più anziani, senza differenze cliniche degne di nota tra i due gruppi di età. Alla fine del periodo di follow-up di 3 mesi, la pressione arteriosa sistolica media e la pressione arteriosa diastolica media erano inferiori all’obiettivo pressorio di < 140/90 mmHg per i singoli pazienti. Nella Figura 2 è possibile osservare come, alla visita, la variazione media della pressione arteriosa sistolica nei pazienti più anziani (> 55 anni) e più giovani (≤ 55 anni) è stata rispettivamente di -16,0 mmHg e -15,5 mmHg, mentre la variazione media della pressione arteriosa diastolica è stata rispettivamente di -7,9 mmHg e -9,0 mmHg. Degno di nota, non vi erano differenze significative tra i gruppi (> 55 anni e ≤ 55 anni). Nella Figura 2 è inoltre possibile osservare, per i due gruppi (> 55 anni e ≤ 55 anni), un’ulteriore diminuzione per entrambe le pressioni alla visita 3, con una variazione media dal basale di -21,6 mmHg e -21,1 mmHg, rispettivamente, per la pressione arteriosa sistolica, e una variazione media dal basale di -10,9 mmHg e -1 2,4 mmHg, rispettivamente, per la pressione arteriosa diastolica. Anche in questo caso, non vi erano differenze tra pazienti più giovani e pazienti più anziani nell’efficacia di riduzione della pressione arteriosa con Barnidipina. La diminuzione della pressione media del polso dopo circa 3 mesi di terapia è stata maggiore nei pazienti > 55 anni (-10,8 mmHg) rispetto ai pazienti ≤ 55 anni (-8,7 mmHg), tendenza già visibile alla visita 2 (-8,2 mmHg e -6,5 mmHg, rispettivamente). La diminuzione della pressione media del polso è stata maggiore nei pazienti > 55 anni (-10,8 mmHg) rispetto ai pazienti ≤ 55 anni (-8,7 mmHg) e la percentuale di pazienti con pressione del polso > 60 mmHg è diminuita dal 61,1% al basale al 24,8% alla visita 3 nei pazienti >55 anni, e dal 47,7% al 16,5% nei pazienti ≤ 55 anni. Per quanto riguarda l’incidenza complessiva degli eventi avversi, questa è risultata essere bassa e ha portato all’interruzione del trattamento solo nel 3,0%-3,6% dei pazienti. L’edema periferico, un effetto avverso comune dei calcio-antagonisti nella pratica clinica, è stato riportato dal 2,7% dei pazienti di età < 65 anni e dal 4,6% dei pazienti di età ≥ 65 anni. Questi risultati supportano quindi sia l’efficacia sia la tollerabilità di Barnidipina nei pazienti più anziani come nei pazienti più giovani.
- Barnidipina può esercitare un effetto favorevole sulla disfunzione endoteliale nei pazienti ipertesi: risultati di uno studio preliminare (28)
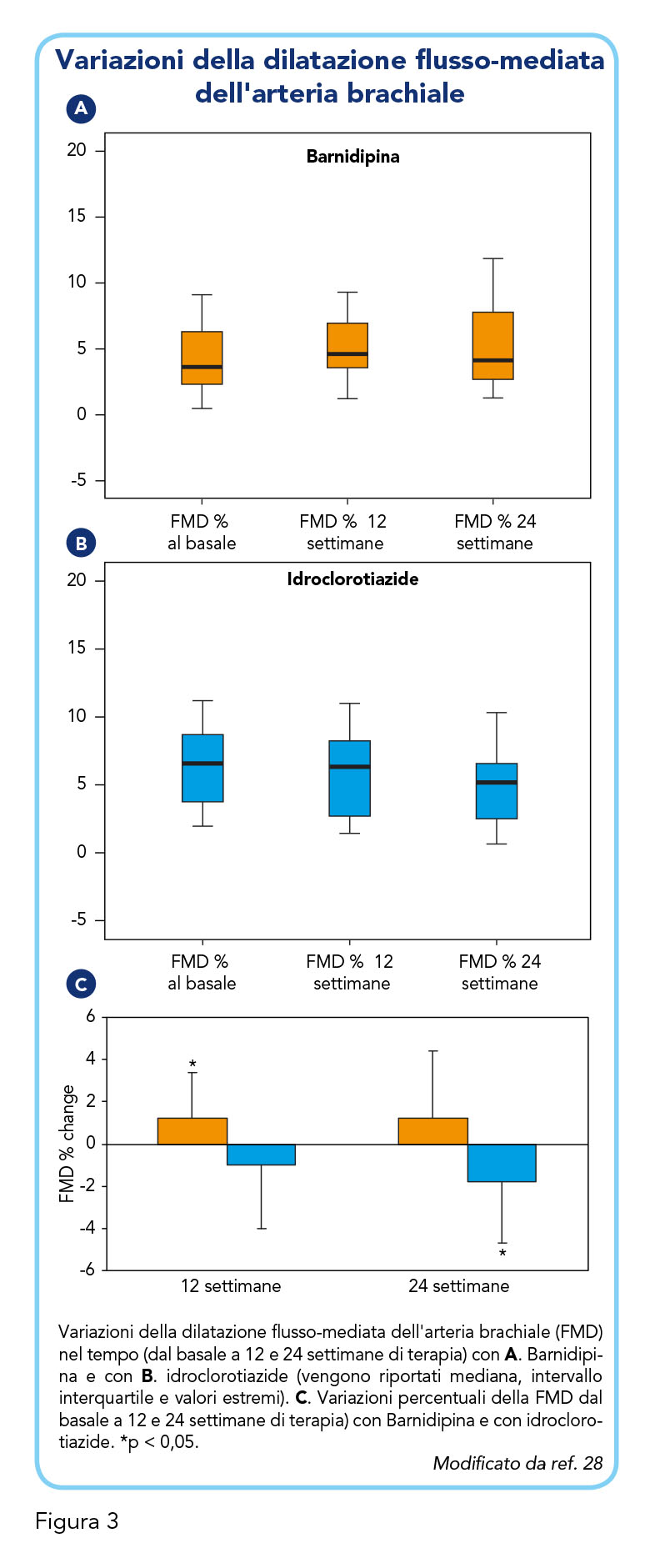
Numerose evidenze dimostrano che l’ipertensione essenziale sia causa di disfunzione endoteliale, caratterizzata da fattori quali lo squilibrio tra vasodilatazione e vasocostrizione e l’aumento dello stress ossidativo che, a loro volta, contribuiscono al danno vascolare, allo sviluppo e alla progressione dell’aterosclerosi e all’insorgenza di eventi cardiovascolari (e.g. 29). Sulla base di questa premessa, uno studio italiano ha indagato gli effetti del trattamento antipertensivo (fino a 24 settimane) con Barnidipina rispetto a un diuretico tiazidico, l’idroclorotiazide, sulla funzione endoteliale in pazienti con ipertensione essenziale da lieve a moderata − pressione arteriosa diastolica da seduti di 90-109 mmHg e/o pressione arteriosa sistolica di 140-179 mmHg. Lo studio era randomizzato a gruppi paralleli, open-label. Dopo 2 settimane di run-in senza trattamento, i pazienti sono stati randomizzati per ricevere Barnidipina alla dose giornaliera iniziale di 10 mg, o idroclorotiazide alla dose iniziale giornaliera di 12,5 mg. Dopo 6 settimane di trattamento, nei pazienti non responsivi al trattamento il dosaggio giornaliero del farmaco è stato raddoppiato, mentre nei pazienti responsivi questo dosaggio è stato mantenuto fino alla fine dello studio (28). La funzione endoteliale è stata misurata attraverso la dilatazione flusso-mediata dell’arteria brachiale (FMD), una tecnica ecografica ad alta risoluzione non invasiva, ben tollerata e riproducibile. Dopo 12 e 24 settimane di trattamento, è stata osservata una riduzione significativa della pressione arteriosa clinica in entrambi i gruppi di trattamento. Inoltre, è stata osservata una riduzione significativa della pressione arteriosa sistolica e della pressione arteriosa diastolica nelle 24 ore nei pazienti che ricevevano Barnidipina, ma non in quelli che ricevevano il diuretico. Per quanto riguarda la funzione endoteliale, innanzitutto va notato che i valori del diametro al basale erano simili e non sono state osservate variazioni durante il trattamento in entrambi i gruppi di pazienti. Il valore medio della FMD misurato al basale, invece, era significativamente più alto nei pazienti sottoposti a terapia diuretica (6,88 ± 3,64% vs 3,9 ± 3,14%, p < 0,05 nei pazienti trattati con idroclorotiazide e Barnidipina, rispettivamente). Dopo 12 settimane di trattamento è stato osservato un significativo aumento della FMD nel gruppo Barnidipina, mentre una lieve riduzione, anche se non statisticamente significativa, della FMD endotelio-dipendente è stata trovata nel gruppo idroclorotiazide. Dopo 24 settimane di trattamento, un ulteriore lieve aumento della dilatazione endotelio-dipendente (anche se non statisticamente significativo rispetto al basale) è stato osservato nel gruppo Barnidipina. La riduzione della FMD osservata nel gruppo idroclorotiazide dopo 12 settimane è stata confermata a 24 settimane di trattamento (Figura 3). La variazione percentuale della FMD era diversa tra i pazienti trattati con Barnidipina (a 12 settimane 1,2 ± 2,2%, p < 0,023 e a 24 settimane 1,25 ± 3,15%, p < 0,16 dal basale) e quelli trattati con idroclorotiazide (a 12 settimane 1,0 ± 3,0%, p < 0,089 e a 24 settimane 1,78 ± 2,9%, p < 0,015 dal basale) (Figura 3). Considerando i valori di FMD prima del trattamento e alla fine dello studio, si può notare un aumento significativo della FMD a 24 settimane durante il trattamento con Barnidipina ma non durante la somministrazione di idroclorotiazide. Nell’intero gruppo, non è stata osservata alcuna correlazione significativa tra le variazioni della FMD e le variazioni della pressione arteriosa sistolica clinica. Al contrario, le variazioni della FMD a 6 mesi erano significativamente correlate alle variazioni del colesterolo LDL e del potassio sierico (28). Questi risultati suggeriscono quindi che, attraverso il trattamento con Barnidipina, ma non con un diuretico, è possibile ottenere un miglioramento della disfunzione endoteliale, valutata mediante ecografia non invasiva della dilatazione dell’arteria brachiale in risposta all’iperemia reattiva. Sebbene questo studio debba considerarsi pilota, a causa del numero ridotto di pazienti studiati, apre nuove prospettive per lo studio di ulteriori benefici di Barnidipina e degli altri calcio-antagonisti (28).
- Miglioramento dei parametri ecocardiografici in seguito a trattamento con Barnidipina in associazione a un sartano (30)
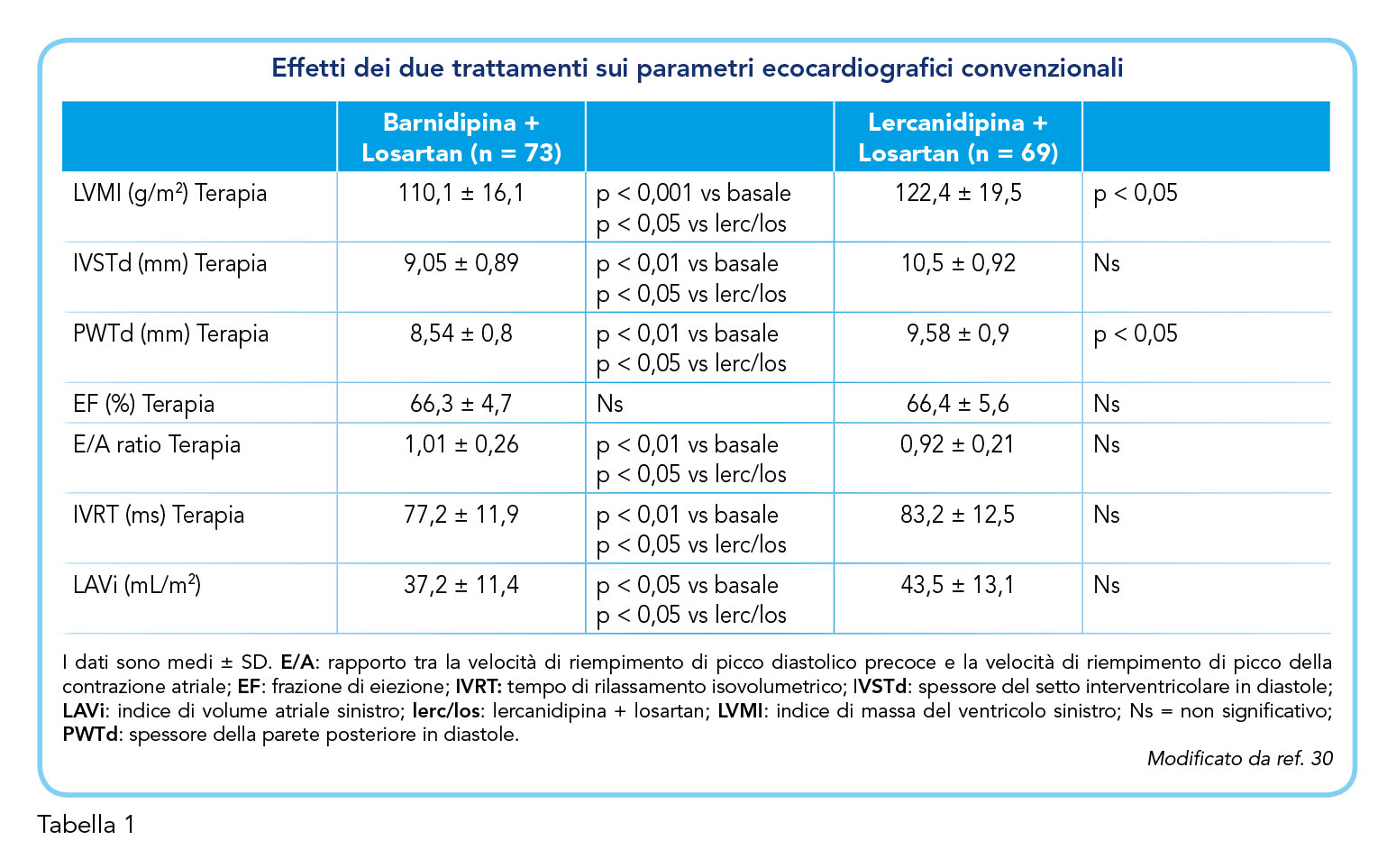
L’ipertrofia ventricolare sinistra (LVH), un marker di danno end-organ cardiaco, si riscontra frequentemente nei pazienti ipertesi ed è altamente predittiva delle complicanze cardiovascolari. Il diabete mellito è uno stimolo indipendente per l’LVH, che a sua volta può contribuire agli eventi cardiovascolari nei soggetti diabetici (31). Quando l’ipertensione è associata al diabete, lo sviluppo di LVH è ulteriormente accelerato e il rischio di complicanze cardiovascolari è quindi notevolmente aumentato. A oggi, il miglior trattamento della LVH è la sua identificazione precoce e la rapida implementazione di un trattamento adeguato: i bloccanti del recettore dell’angiotensina II (ARBs o sartani) e gli inibitori dell’enzima di conversione dell’angiotensina (ACE-inibitori) dovrebbero essere la terapia di prima linea, poiché si sono dimostrati i più efficaci nel ridurre l’LVH nei pazienti diabetici di tipo 2. Nei casi in cui gli ACE-inibitori o gli ARBs siano controindicati o non tollerati, o quando non sono sufficienti per raggiungere un adeguato controllo della pressione arteriosa, si dovrebbe aggiungere un altro agente antipertensivo, e i calcio-antagonisti potrebbero essere un’opzione come terapia di seconda linea (32). Questo studio ha quindi valutato gli effetti di Lercanidipina, un altro calcio-antagonista, rispetto a Barnidipina, entrambi in aggiunta a Losartan, su alcuni parametri ecocardiografici, in pazienti ipertesi, diabetici di tipo 2, con LVH. In questo studio italiano, multicentrico, randomizzato, in doppio cieco e controllato sono stati inclusi pazienti adulti con ipertensione da lieve a moderata, con diabete mellito di tipo 2, con LVH, non ben controllati da Losartan, con colesterolo lipoproteico a bassa densità (LDL) < 160 mg/dL, ambulatoriali in sovrappeso. I pazienti sono stati randomizzati a Lercanidipina 20 mg/die o Barnidipina 20 mg/die, in aggiunta a Losartan 100 mg/die per 6 mesi (30). Degno di nota, nessun paziente ha interrotto lo studio a causa di eventi avversi. Entrambi i trattamenti hanno indotto una riduzione simile e significativa rispetto al basale della pressione arteriosa sistolica e della pressione arteriosa diastolica, senza differenze statisticamente significative tra i due gruppi. Per quanto riguarda i parametri metabolici, il colesterolo LDL è stato ridotto da Barnidipina + Losartan, sia rispetto al basale che rispetto a Lercanidipina + Losartan, e l’acido urico è stato ridotto in entrambi i gruppi rispetto al basale (quest’ultimo effetto probabilmente dovuto all’assunzione concomitante di Losartan). L’indice di massa ventricolare sinistra, utilizzato come misura dell’LVH, è stato ridotto da entrambi i trattamenti, ma in misura maggiore da Barnidipina + Losartan (Tabella 1). Anche lo spessore del setto interventricolare in diastole è stato ridotto da Barnidipina + Losartan sia rispetto al basale che rispetto a Lercanidipina + Losartan (Tabella 1). Per tutti gli altri parametri presi inconsiderazione (Tabella 1) − riduzione dello spessore della parete posteriore in diastole; aumento del rapporto tra la velocità di riempimento diastolico precoce di picco e della velocità di riempimento di picco della contrazione atriale; riduzione del tempo di rilassamento isovolumetrico; riduzione dell’indice di volume atriale sinistro −, solo Barnidipina + Losartan sono stati efficaci, sia rispetto al basale che contro Lercanidipina + Losartan (30). Questi risultati dimostrano quindi innanzitutto che Barnidipina ha migliorato il colesterolo LDL. Poiché il dosaggio degli agenti ipocolesterolemizzanti che assumevano i pazienti, in sovrappeso, è stato mantenuto stabile durante tutto lo studio, gli effetti sul profilo lipidico sembrano essere strettamente legati a Barnidipina. Importante, questo studio dimostra un effetto positivo di Barnidipina sui parametri ecocardiografici, più efficace di Lercanidipina, con miglioramento dell’indice di massa ventricolare sinistra, dello spessore del setto interventricolare in diastole, dello spessore della parete posteriore in diastole e del tempo di rilassamento isovolumetrico. Questa differenza rispetto a uno studio precedente (33) è probabilmente dovuta alla maggiore durata del presente studio, 6 mesi vs 3 mesi. Inoltre, questo effetto positivo sui parametri ecocardiografici non sembra essere correlato alla riduzione della pressione arteriosa, perché anche il trattamento con Lercanidipina ne ha migliorato il controllo. Gli autori concludono che Barnidipina abbia probabilmente un’efficacia protettiva degli organi finali più pronunciata legata alle caratteristiche intrinseche di questo composto.
Conclusioni
Barnidipina è un calcio-antagonista lipofilo diidropiridinico indicato nel trattamento dell’ipertensione essenziale da lieve a moderata. Il dosaggio di Barnidipina una volta al giorno, la sua buona tollerabilità e l’effetto antipertensivo duraturo e dose-dipendente contribuiscono a un’ottima aderenza dei pazienti. Barnidipina è caratterizzata da una lenta insorgenza d’azione e da un legame forte e duraturo con i canali del calcio di tipo L. L’efficacia e la tollerabilità di Barnidipina sono comprovatamente comparabili in pazienti più giovani e pazienti più anziani. Uno studio pilota, inoltre, suggerisce che Barnidipina possa avere un effetto benefico sulla disfunzione endoteliale. Infine, Barnidipina in associazione a un sartano migliora i parametri ecocardiografici indipendentemente dalla riduzione della pressione arteriosa.
Bibliografia
- Zhou B, Carrillo-Larco RM, Danaei G, Riley LM, Paciorek CJ, Stevens GA, et al. Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. The Lancet. 2021 Sep 11;398(10304):957–80.
- Tocci G, Battistoni A, Passerini J, Musumeci MB, Francia P, Ferrucci A, et al. Calcium channel blockers and hypertension. J Cardiovasc Pharmacol Ther. 2015 Mar;20(2):121–30.
- Lewington S, Clarke R, Qizilbash N, Peto R, Collins R, Prospective Studies Collaboration. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet. 2002 Dec 14;360(9349):1903–13.
- More than 700 million people with untreated hypertension [Internet]. World Health Organization (WHO); 2021. Available from: https://www.who.int/news/item/25-08-2021-more-than-700-million-people-with-untreated-hypertension
- Volpe M. Calcium Channel Blockers for the Clinical Management of Hypertension. High Blood Press Cardiovasc Prev. 2018 Mar;25(1):1–3.
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. J Hypertens. 2018 Oct;36(10):1953–2041.
- Godfraind T. Discovery and Development of Calcium Channel Blockers. Frontiers in Pharmacology [Internet]. 2017 [cited 2022 Sep 23];8. Available from: https://www.frontiersin.org/articles/10.3389/fphar.2017.00286
- Elliott WJ, Ram CVS. Calcium channel blockers. J Clin Hypertens (Greenwich). 2011 Sep;13(9):687–9.
- Ambrosioni E, Borghi C. Calcium channel antagonists in hypertension. Am J Hypertens. 1989 Feb;2(2 Pt 2):90S-93S.
- Yokoyama S, Kaburagi T. Clinical effects of intravenous nifedipine on renal function. J Cardiovasc Pharmacol. 1983 Feb;5(1):67–71.
- van Zwieten PA, van Meel JC, Timmermans PB. Pharmacology of calcium entry blockers: interaction with vascular alpha-adrenoceptors. Hypertension. 1983;5(4 Pt 2):II8-17.
- Pasanisi F, Elliott HL, Meredith PA, Sumner DJ, Reid JL. Effect of calcium channel blockers on adrenergic and nonadrenergic vascular responses in man. J Cardiovasc Pharmacol. 1985;7(6):1166–70.
- Staessen JA, Fagard R, Thijs L, Celis H, Arabidze GG, Birkenhäger WH, et al. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. The Systolic Hypertension in Europe (Syst-Eur) Trial Investigators. Lancet. 1997 Sep 13;350(9080):757–64.
- Liu L, Zhang Y, Liu G, Li W, Zhang X, Zanchetti A, et al. The Felodipine Event Reduction (FEVER) Study: a randomized long-term placebo-controlled trial in Chinese hypertensive patients. J Hypertens. 2005 Dec;23(12):2157–72.
- Dahlöf B, Hansson L, Lindholm LH, Scherstén B, Wester PO, Ekbom T, et al. STOP-Hypertension 2: a prospective intervention trial of “newer” versus “older” treatment alternatives in old patients with hypertension. Swedish Trial in Old Patients with Hypertension. Blood Press. 1993 Jun;2(2):136–41.
- Brown MJ, Palmer CR, Castaigne A, de Leeuw PW, Mancia G, Rosenthal T, et al. Morbidity and mortality in patients randomised to double-blind treatment with a long-acting calcium-channel blocker or diuretic in the International Nifedipine GITS study: Intervention as a Goal in Hypertension Treatment (INSIGHT). Lancet. 2000 Jul 29;356(9227):366–72.
- Malacco E, Mancia G, Rappelli A, Menotti A, Zuccaro MS, Coppini A, et al. Treatment of isolated systolic hypertension: the SHELL study results. Blood Press. 2003;12(3):160–7.
- Malhotra HS, Plosker GL. Barnidipine. Drugs. 2001;61(7):989-996. doi:0012-6667/01/0007-0989/$27.50/0
- Liau CS. Barnidipine: A new calcium channel blocker for hypertension treatment. Expert Rev Cardiovasc Ther. 2005;3(2):207-213. doi:10.1586/14779072.3.2.207
- Janssen BJA, Kam KL, Smits JFM. Preferential renal and mesenteric vasodilation induced by barnidipine and amlodipine in spontaneously hypertensive rats. Naunyn-Sclrn1iedeberg’s Arch Pharmacol. 2001;364:414-421. doi:l 0.1007 /s002 l 00 l 00468
- Teramura T, Watanabe T, Higuchi S, Hashimoto K. Metabolism and pharmacokinetics of barnidipine hydrochloride, a calcium channel blocker, in man following oral administration of its sustained release formulation. http://dx.doi.org/101080/004982597240695. 2008;27(2):203-216. doi:10.1080/004982597240695
- Wegener JW, Meyrer H, Rupp J, Nawrath H. Barnidipine block of L-type Ca2+ channel currents in rat ventricular cardiomyocytes. Br J Pharmacol. 2000;130(8):2015-2023. doi:10.1038/SJ.BJP.0703514
- Lins R, de Vries C. Efficacy and Tolerability of Barnidipine in Real-Life Arterial Hypertension: Results from Younger and Older Patients in the BASIC-BT Study. The Open Cardiovasculur Medicine Jourual. Published online 2017.
- Naber FB, Häge R, Mortelmans J. Barnidipine monotherapy and combination therapy in older patients with essential hypertension: a long-term study. Int J Clin Pract Suppl. 2000;114:27-35.
- Otterstad JE, Ruilope LM. Treatment of hypertension in the very old. Int J Clin Pract Suppl. 2000;114.
- Lins R, Marckx P, Vandebeek R, Vanhoutvinck C, Neuville O. Barnidipine real-life tolerability in arterial hypertension: results from the BASIC-HT study. http://dx.doi.org/101179/2295333715Y0000000012. 2015;70(4):244-250. doi:10.1179/2295333715Y.0000000012
- (UK) NCGC. Hypertension. NICE. Published online 2011. Accessed October 17, 2022. https://www.ncbi.nlm.nih.gov/books/NBK83274/
- Muiesan ML, Salvetti M, Belotti E, et al. Effects of barnidipine in comparison with hydrochlorothiazide on endothelial function, as assessed by flow mediated vasodilatation in hypertensive patients. Blood Press. 2011;20(4):244-251. doi:10.3109/08037051.2011.561072
- Muiesan ML, Salvetti M, Paini A, et al. Prognostic role of flow-mediated dilatation of the brachial artery in hypertensive patients. J Hypertens. 2008;26(8):1612-1618. doi:10.1097/HJH.0B013E328304B083
- Derosa G, Mugellini A, Querci F, et al. Barnidipine or Lercanidipine on Echocardiographic Parameters in Hypertensive, Type 2 Diabetics with Left Ventricular Hypertrophy: A Randomized Clinical Trial. Sci Rep. 2015;5. doi:10.1038/srep12603
- Nielsen FS et al. Left ventricular hypertrophy in non-insulin-dependent diabetic patients with and without diabetic nephropathy. Diabet Med. 1997;14:538-546.
- Derosa G, Maffioli P. Assessment and management of left ventricular hypertrophy in Type 2 diabetes patients with high blood pressure. http://dx.doi.org/101586/erc1336. 2014;11(6):719-728. doi:10.1586/ERC.13.36
- Angell F, Repaci S, Borgioni C, Sardone M, Scotti A, Verdecchia P. Effects of barnidipine on blood pressure and left ventricular diastolic function in patients with hypertension and metabolic syndrome: A 12-week, open-label noncomparison study. Current Therapeutic Research. 2008;69(3):207-220. doi:10.1016/J.CURTHERES.2008.06.003
- Ipertensione: stato dell’arte
Uno studio dell’Imperial College di Londra, pubblicato su The Lancet nel 2021, afferma che il numero di adulti tra i 30 e i 79 anni affetti da ipertensione a livello globale è aumentato da 650 milioni a 1,28 miliardi negli ultimi trent’anni (1). L’ipertensione è un importante fattore di rischio modificabile, che aumenta significativamente la possibilità di sviluppare complicanze cardiovascolari, cerebrovascolari e renali (2,3). Ciononostante, sono oltre 700 milioni i soggetti ipertesi a non ricevere trattamento (4) e, tra quelli trattati, solo il 20-30% raggiunge i valori raccomandati di pressione sanguigna (2). L’ipertensione incontrollata è persistentemente responsabile della maggioranza delle malattie cardiovascolari tra cui infarto miocardico, ictus ischemico e insufficienza cardiaca congestizia, determinando così un elevato numero di decessi per cause cardiovascolari in vari Paesi, inclusa l’Italia (2,5). Le linee guida ESC/ESH hanno fissato, come valori soglia oltre cui si è definiti ipertesi, 140 mmHg per la pressione sistolica e 90 mmHg per la pressione diastolica (6). Il raggiungimento di valori al di sotto di questa soglia è raccomandato indipendentemente da genere d’appartenenza, età, etnia o condizione clinica concomitante (2).
Seguire una terapia antipertensiva previene morbilità e mortalità cardiovascolare ed è compito del clinico spronare il paziente affinché quest’ultimo aderisca al trattamento assegnatogli, incentivandolo inoltre a modificare il suo stile di vita e a prendersi cura delle condizioni di comorbilità che possono peggiorarne la salute complessiva e la qualità della vita. Circa la metà degli individui in terapia antipertensiva interrompe spontaneamente il farmaco prescritto, indipendentemente dal raggiungimento dei livelli pressori raccomandati, spesso anche a causa di una mancata tollerabilità nei confronti del farmaco assegnato (5). Scegliere il giusto farmaco per ogni paziente è infatti fondamentale e il clinico deve dunque conoscere e selezionare la terapia più adatta ad ogni situazione e caso clinico. Non solo esistono svariate classi di farmaci antipertensivi, con meccanismi d’azione ben distinti, ma vi è anche un’ampia scelta di composti all’interno di ciascuna di queste classi, e le specifiche proprietà di ciascuno di questi può determinare un diverso esito clinico. Tra gli agenti antipertensivi raccomandati in prima linea per il trattamento dell’ipertensione troviamo: gli inibitori dell’enzima di conversione dell’angiotensina (noti come ACE-inibitori), gli antagonisti del recettore dell’angiotensina (noti come sartani o ARBs, Angiotensin Receptor Blockers), i beta-bloccanti, i diuretici e, infine, i calcio-antagonisti, oggetto di approfondimento in questo numero di PCR.
- Farmaci calcio-antagonisti
I calcio-antagonisti sono tra i farmaci raccomandati in prima linea per il trattamento dell’ipertensione e delle comorbidità correlate, e sono ideali sia per l’utilizzo in monoterapia che in doppia o tripla combinazione con altri agenti antipertensivi (2). Essi agiscono sui canali voltaggio-dipendenti di tipo L degli ioni calcio – dove “L” sta per “long-lasting”, riferendosi alla durata dell’attivazione del canale – posizionati sulla membrana di cellule della muscolatura liscia dei vasi sanguigni e di cellule cardiache. Se stimolati, questi canali si aprono permettendo l’afflusso degli ioni calcio all’interno della cellula (depolarizzazione) e innescando la contrazione delle fibre di actina e miosina. I calcio-antagonisti (o bloccanti dei canali del calcio) bloccano, per l’appunto, l’apertura del canale inibendo lo stimolo alla contrazione. La scoperta di questa classe di farmaci è scaturita da uno studio farmacologico degli anni ’60 che valutava varie molecole per la dilatazione coronarica (7). I calcio-antagonisti agiscono rilassando le cellule muscolari lisce dei vasi sanguigni, favorendo la vasodilatazione, riducendo la resistenza vascolare e, perciò, riducendo la pressione sanguigna (8). Tale azione vasodilatatoria può inoltre favorire la natriuresi attraverso l’aumento del flusso sanguigno a livello renale, la dilatazione delle arteriole afferenti e l’aumento della pressione di filtrazione glomerulare (8–10). Vi sono oltretutto evidenze che i calcio-antagonisti interferiscano con l’attività a-adrenergica che regola la contrattilità della muscolatura liscia, meccanismo che potrebbe ulteriormente contribuire all’effetto vasodilatatorio di questa classe di farmaci (9,11,12).
I calcio-antagonisti sono una classe eterogenea, ne esistono infatti tre gruppi definiti dall’affinità ai canali del calcio vascolari e cardiaci. La classe attualmente più comune è quella degli agenti diidropiridinici, che agiscono prevalentemente come dilatatori dei vasi periferici; le altre due classi sono i fenilalchilaminici, attivi a livello cardiaco, e i benzotiazepinici, che hanno un profilo d’affinità intermedio (5). Nel corso degli anni, molti studi clinici hanno dimostrato la capacità dei calcio-antagonisti di ridurre mortalità e morbilità cardiovascolare (2). Lo studio Syst-Eur (Systolic Hypertension in Europe), ideato per valutare i benefici cardiovascolari dell’impiego di un calcio-antagonista appartenente al gruppo delle diidropiridine, è stato interrotto dopo circa 2 anni per l’evidente riduzione del tasso di complicanze cardiovascolari nel gruppo assegnato al trattamento attivo rispetto al placebo (13). Lo studio FEVER (Felodipine EVEnt Reduction) ha anch’esso dimostrato la sostanziale riduzione di eventi cardiovascolari gravi e di mortalità nei pazienti in trattamento con un altro calcio-antagonista diidropiridinico, rispetto al placebo (14). Nel confronto, invece, tra calcio-antagonisti e altri agenti antipertensivi, svariati studi hanno attestato la validità del beneficio di protezione cardiovascolare conseguente all’impiego di farmaci calcio-antagonisti. È il caso, ad esempio, degli studi STOP Hypertension-2 (Swedish Trial in Old Patients with Hypertension-2 Study), INSIGHT (International Nifedipine GITS Study: Intervention as a Goal in Hypertension Treatment) e SHELL (Systolic Hypertension in the Elderly), che hanno riportato un’efficacia antipertensiva e di prevenzione da ictus equivalente ad alcuni farmaci comunemente impiegati nel trattamento dell’ipertensione (15–17). Alcuni di questi studi prevedevano inoltre terapie combinate con più agenti antipertensivi, al fine di valutare le combinazioni più efficaci a questo scopo. In sintesi, i calcio-antagonisti hanno comprovate evidenze di riduzione di morbilità e di mortalità cardiovascolare, sia in monoterapia che in combinazione ad altri agenti antipertensivi, e sono per questo raccomandati per il trattamento dell’ipertensione dalle linee guida ESC/ESH (2,6). Insieme ai farmaci inibitori del sistema renina-angiotensina, i calcio-antagonisti sono attualmente tra le strategie antipertensive più efficaci e meglio tollerate rispetto ad altre classi di farmaci (2). Come raccomandato dalle linee guida ESC/ESH, nei pazienti che non raggiungono i valori pressori target in monoterapia, calcio-antagonisti e farmaci inibitori del sistema renina-angiotensina possono essere combinati al fine di ottenere un miglior controllo pressorio (6). In questo contesto, le due classi di farmaci esistono anche in singole formulazioni a combinazione fissa al fine di favorire l’aderenza alla terapia. Nei casi in cui anche il duplice approccio non dovesse rivelarsi sufficientemente efficace, è possibile passare a una triplice terapia che coniuga calcio-antagonisti, inibitori del sistema renina-angiotensina e diuretici, al fine di massimizzare l’azione sinergica per raggiungere l’efficacia antipertensiva attraverso molteplici meccanismi d’azione (6).
- Barnidipina
3.1. Indicazioni e posologia
Barnidipina è un calcio-antagonista diidropiridinico che, come altri membri di questa classe di farmaci, è selettivo per i canali del calcio di tipo L (ad azione prolungata) ed è composta da un singolo isomero ottico (configurazione S,S). La struttura molecolare di Barnidipina è mostrata nella Figura 1. Barnidipina produce il suo effetto antipertensivo bloccando selettivamente l’afflusso di ioni calcio attraverso i canali “voltaggio-dipendenti” di tipo L nelle membrane eccitabili delle cellule muscolari lisce vascolari, come risultato dell’interazione con specifici recettori dei canali del calcio di tipo L, provocando vasodilatazione e conseguente riduzione delle resistenze periferiche (18-20). Barnidipina è disponibile in una formulazione a rilascio modificato per somministrazione orale una volta al giorno nel trattamento di pazienti con ipertensione essenziale da lieve a moderata. Le capsule vanno assunte preferibilmente con un bicchiere d’acqua, prima, durante o dopo i pasti.
La dose iniziale di Barnidipina raccomandata in RCP è di 10 mg una volta al giorno al mattino, ma può essere aumentata a 20 mg una volta al giorno, se necessario. Tuttavia, la decisione di aumentare la dose deve essere presa solo dopo aver ottenuto una completa stabilità dei valori pressori con la dose iniziale, che di solito avviene dopo 3-6 settimane. Poiché non sono disponibili dati nei bambini (< 18 anni), Barnidipina non deve essere somministrata nella popolazione pediatrica. La dose non deve essere aggiustata in pazienti anziani, anche se in questa popolazione è raccomandata una maggiore attenzione all’inizio del trattamento. Nei pazienti con compromissione renale da lieve a moderata bisogna prestare attenzione quando si aumenta la dose da 10 a 20 mg una volta al giorno.
3.2. Meccanismo d’azione
Barnidipina è un calcio antagonista lipofilo diidropiridinico caratterizzato da una lenta insorgenza d’azione e da un legame forte e duraturo con i canali del calcio di tipo L. Barnidipina mostra un’elevata affinità per i canali espressi nelle cellule muscolari lisce della parete vascolare, per cui il suo principale meccanismo d’azione deriva dalla riduzione della resistenza vascolare periferica secondaria alla sua azione vasodilatatoria. L’afflusso di ioni calcio attraverso canali “voltaggio-dipendenti” di tipo L nelle membrane eccitabili delle cellule muscolari lisce promuove la formazione di ponti incrociati calcio-dipendenti tra miosina e actina, le due principali proteine contrattili che guidano la contrazione. Bloccando i canali del calcio di tipo L “voltaggio-dipendenti”, Barnidipina blocca selettivamente l’afflusso di ioni calcio nelle cellule muscolari lisce e inibisce l’attivazione delle proteine contrattili (21,22). Come altri calcio-antagonisti diidropiridinici, si ipotizza che Barnidipina interagisca con la subunità alfa 1-C dei canali del calcio di tipo L, e che la subunità alfa 1-C del canale risieda all’interno del poro a doppio strato o del poro del canale, in una posizione più vicina alla superficie extracellulare che a quella intracellulare della membrana. Si ritiene che la lipofilia sia la probabile ragione di questa interazione e il motivo probabile per cui Barnidipina mostra un inizio lento e una lunga durata d’azione. Essendo una molecola altamente lipofila con un coefficiente di ripartizione ottanolo/acqua pari a 2.000, ci si aspetta che Barnidipina si accumuli nella membrana cellulare e, di conseguenza, acceda al suo recettore bersaglio in modo lento (21,22).
3.3. Farmacocinetica
Barnidipina è prontamente assorbita dal tratto gastrointestinale, ma subisce un esteso metabolismo di primo passaggio. La biodisponibilità assoluta della formulazione a rilascio modificato di Barnidipina valutata dopo una singola infusione di 6 ore da 0,75 mg e dopo una singola dose orale da 20 mg in volontari sani è stata dell’1,1%. La biodisponibilità della formulazione a rilascio modificato di Barnidipina, inoltre, non è influenzata in modo significativo dall’assunzione di cibo in volontari sani, né la farmacocinetica di questa formulazione è influenzata dall’età, dal sesso o dalla funzione renale (18). Il legame in vitro di Barnidipina con le proteine plasmatiche, principalmente con l’albumina, è compreso tra il 92,4% e il 98,9%. I test di legame con le proteine non hanno mostrato interazioni con farmaci quali amitriptilina, diazepam, diclofenac, fenitoina e warfarin. L’area sotto la curva della concentrazione plasmatica (AUC) ottenuta con la formulazione a rilascio modificato (2,85 μg/L∙h) è pari al 97% di quella ottenuta con la formulazione convenzionale in uno studio crossover condotto su volontari sani. La concentrazione plasmatica di picco di Barnidipina dopo una singola dose da 10 mg della formulazione a rilascio modificato è stata di 0,48 μg/L∙h. Dopo la somministrazione di singole dosi orali di Barnidipina radiomarcata nei ratti, i livelli di radioattività sono risultati più elevati nel rene, nel fegato e nel tratto gastrointestinale rispetto al plasma, mentre il cervello ha mostrato il livello più basso di radioattività (1).
3.4. Sicurezza e tollerabilità
Barnidipina è controindicata in caso di: ipersensibilità al principio attivo (o a una qualsiasi altra diidropiridina) o a uno qualsiasi degli eccipienti; grave compromissione renale (clearance della creatinina < 10 mL/min); angina pectoris instabile e infarto miocardico acuto (nelle prime 4 settimane); insufficienza cardiaca non in trattamento. I livelli ematici di Barnidipina possono aumentare quando viene usata in associazione con potenti inibitori del CYP3A4 (come risulta da studi di interazione in vitro), motivo per cui non va usata in associazione ad antiproteasici, ketoconazolo, itraconazolo, eritromicina e claritromicina. Si consiglia cautela nell’uso concomitante di deboli inibitori o induttori del CYP3A4. In caso di uso concomitante con inibitori del CYP3A4 si sconsiglia di aumentare il dosaggio di Barnidipina a 20 mg. Si consiglia inoltre cautela nell’uso concomitante di Barnidipina e cimetidina.
La contemporanea somministrazione di Barnidipina e di altri antipertensivi può determinare un effetto antipertensivo addizionale. Barnidipina può essere impiegato in concomitanza con beta-bloccanti o ACE-inibitori. Altre possibili interazioni farmacologiche potrebbero non essere note per mancanza di studi dedicati.
Barnidipina deve essere impiegato con cautela in pazienti con compromissione renale da lieve a moderata (clearance della creatinina compresa fra 10 e 80 mL/min). L’associazione di un calcio-antagonista con un farmaco che esercita un effetto inotropo negativo può provocare scompenso cardiaco, ipotensione o un (altro) infarto miocardico in pazienti ad alto rischio (ad es. pazienti con anamnesi di infarto miocardico). Come per tutti i derivati diidropiridinici, anche Barnidipina va usato con cautela in pazienti con disfunzione ventricolare sinistra, in pazienti con ostruzione del canale di efflusso del ventricolo sinistro e in pazienti con scompenso isolato del cuore destro. Barnidipina non è stata studiata in pazienti di classe III o IV della New York Heart Association Functional Classification (NYHA). È raccomandata cautela anche quando Barnidipina viene somministrata a pazienti con malattia del nodo del seno (in assenza di pacemaker).
Una dose più elevata di Barnidipina può essere necessaria quando viene somministrata in concomitanza con farmaci induttori enzimatici, come fenitoina, carbamazepina e rifampicina. Qualora il paziente dovesse smettere di usare un farmaco induttore enzimatico, si deve prendere in considerazione la riduzione della dose di Barnidipina. In base ai risultati di studi di interazione in vitro con (fra gli altri) simvastatina, metoprololo, diazepam e terfenadina, si ritiene improbabile che Barnidipina abbia effetti sulla farmacocinetica di altri farmaci che vengono metabolizzati dagli isoenzimi del citocromo P450.
Uno studio di interazione in vivo ha dimostrato che Barnidipina non influenza la farmacocinetica della digossina. In uno studio di interazione, l’alcool ha determinato un aumento dei livelli plasmatici di Barnidipina (40%), che non viene considerato clinicamente rilevante. Come con tutti i vasodilatatori e gli antipertensivi, si deve prestare cautela nell’assunzione concomitante di alcool poiché esso potrebbe potenziarne gli effetti. Nonostante la cinetica di Barnidipina non sia stata modificata significativamente dalla somministrazione di succo di pompelmo, è stato osservato un modico effetto.
Non esistono dati clinici sull’uso di Barnidipina in gravidanza o durante l’allattamento e studi sugli animali non suggeriscono effetti dannosi diretti, ma solo indiretti, sulla gravidanza né sullo sviluppo dell’embrio/fetale o postnatale. La classe delle diidropiridine ha mostrato la potenzialità di prolungare il travaglio e il parto, che non sono stati osservati con Barnidipina. Pertanto Barnidipina può essere usata in gravidanza solo se il beneficio giustifica il rischio potenziale per il feto. Studi sugli animali hanno inoltre dimostrato che Barnidipina (o i suoi metaboliti) viene escreto nel latte umano, motivo per il quale l’allattamento al seno non è consigliato durante l’uso di questo farmaco. Non sono stati effettuati studi sugli effetti di Barnidipina sulla capacità di guidare veicoli e di utilizzare macchinari, ma si consiglia comunque cautela, in quanto capogiri o vertigini possono presentarsi durante un trattamento antipertensivo.
Tra gli effetti indesiderati noti (da comuni a molto comuni in base al dosaggio) si annoverano cefalea, capogiri/vertigini, palpitazioni, vampate di calore ed edema periferico. I sintomi tendono a diminuire o a scomparire durante il trattamento (entro 1 mese l’edema periferico ed entro 2 settimane le vampate di calore, la cefalea e le palpitazioni). Sebbene non sia stata mai osservata, l’iperplasia gengivale può essere rilevante come avviene con l’impiego di altre diidropiridine. Alcune diidropiridine possono raramente causare dolore precordiale ed angina pectoris. Molto raramente pazienti con preesistente angina pectoris potrebbero osservare aumentata frequenza, durata e gravità di tali attacchi. Potrebbero osservarsi casi isolati di infarto miocardico.
I sintomi clinici dopo un sovradosaggio di calcio-antagonisti si sviluppano entro 30-60 minuti dopo la somministrazione di una dose da 5 a 10 volte superiore alla dose terapeutica. Possono essere teoricamente previsti i seguenti effetti collaterali: ipotensione, effetti elettrofisiologici (bradicardia sinusale, prolungamento della conduzione AV, blocco AV di II e III grado, tachicardia), effetti sul sistema nervoso centrale (sonnolenza, confusione e, raramente, convulsioni), sintomi gastrointestinali (nausea e vomito) ed effetti metabolici (iperglicemia). Il trattamento ospedaliero è necessario nell’eventualità di un’intossicazione. Sono indicati il trattamento sintomatico e il monitoraggio continuo dell’ECG. Nell’eventualità di un sovradosaggio, la lavanda gastrica deve essere eseguita il più presto possibile. Deve essere praticata un’iniezione endovenosa (alla dose di 0,2 mL/kg di peso corporeo) di calcio (preferibilmente 10 mL di una soluzione di cloruro di calcio al 10%) nel corso di 5 minuti, fino a una dose totale di 10 mL al 10%. La contrattilità del miocardio, il ritmo sinusale e la conduzione atrioventricolare verranno quindi migliorati. Il trattamento può essere ripetuto ogni 15-20 minuti (fino a un totale di 4 dosi) in base alla risposta del paziente, controllando i livelli di calcio.
3.5. Studi
- Sottoanalisi dello studio BASIC-HT (23): efficacia e tollerabilità di Barnidipina sono comparabili nei pazienti con ipertensione arteriosa giovani e anziani secondo dati di real-life
In generale, Barnidipina ha dimostrato di essere un farmaco antipertensivo efficace nella gestione dell’ipertensione essenziale nei pazienti anziani (18,24) senza subire l’influenza negativa dell’età (25). La sua tollerabilità è considerata generalmente molto buona nella maggior parte dei pazienti, compresi gli over 75 (18,24,25). La tollerabilità e l’efficacia di Barnidipina (10 mg o 20 mg) sono state studiate, nel 2015, in uno studio osservazionale prospettico su larga scala, open-label, in pazienti con ipertensione essenziale, compresi pazienti con concomitante diabete mellito (n=20.275) (BASIC-HT; BArnidipine real-life Safety and tolerability In Chronic HyperTension) (26). I risultati hanno confermato l’efficacia di Barnidipina nel contesto reale della pratica clinica di routine nella riduzione della pressione arteriosa: questo effetto sembrava inoltre essere dovuto alla buona aderenza alla terapia da parte dei pazienti. I risultati hanno anche mostrato il buon profilo di tollerabilità di Barnidipina (26). Due anni dopo, gli autori hanno pubblicato uno studio − analisi di sottogruppo per età pre-specificate nel protocollo − in cui descrivono l’efficacia e la tollerabilità del trattamento con Barnidipina, sia in monoterapia che in combinazione, in pazienti anziani rispetto a quelli più giovani. I dati relativi alla pressione arteriosa e alla frequenza cardiaca sono stati valutati nei sottogruppi di pazienti di età ≤ 55 anni rispetto a quelli di età > 55 anni: questo cut-off dell’età è di specifica importanza per l’obiettivo della pressione arteriosa e per la scelta del farmaco come trattamento di prima linea secondo le linee guida internazionali (27). In particolare, la maggior parte dei pazienti aveva un’età superiore ai 55 anni (n=14.023; 71,7%; età media: 69,3 anni), circa un quarto dei pazienti (n=4.778; 24,4%) aveva un’età compresa tra i 55 e i 64 anni, e circa la metà dei pazienti aveva un’età ≥ 65 anni (n=9.245; 47,3%): di questi ultimi, n=3.597 pazienti (18,4%) avevano più di 75 anni. La frequenza degli eventi avversi è stata ripartita in base alle fasce d’età dei pazienti < 65 anni e ≥ 65 anni perché questi ultimi hanno maggiori probabilità di sviluppare eventi avversi comuni a molti calcio-antagonisti, tra cui edema, ed eventi avversi cardiaci, come tachicardia e/o palpitazioni. Dai risultati al follow-up di 3 mesi è emersa una riduzione statisticamente significativa, e altrettanto clinicamente importante, della pressione arteriosa sistolica e della pressione arteriosa diastolica sia nei pazienti più giovani che in quelli più anziani, senza differenze cliniche degne di nota tra i due gruppi di età. Alla fine del periodo di follow-up di 3 mesi, la pressione arteriosa sistolica media e la pressione arteriosa diastolica media erano inferiori all’obiettivo pressorio di < 140/90 mmHg per i singoli pazienti. Nella Figura 2 è possibile osservare come, alla visita, la variazione media della pressione arteriosa sistolica nei pazienti più anziani (> 55 anni) e più giovani (≤ 55 anni) è stata rispettivamente di -16,0 mmHg e -15,5 mmHg, mentre la variazione media della pressione arteriosa diastolica è stata rispettivamente di -7,9 mmHg e -9,0 mmHg. Degno di nota, non vi erano differenze significative tra i gruppi (> 55 anni e ≤ 55 anni). Nella Figura 2 è inoltre possibile osservare, per i due gruppi (> 55 anni e ≤ 55 anni), un’ulteriore diminuzione per entrambe le pressioni alla visita 3, con una variazione media dal basale di -21,6 mmHg e -21,1 mmHg, rispettivamente, per la pressione arteriosa sistolica, e una variazione media dal basale di -10,9 mmHg e -1 2,4 mmHg, rispettivamente, per la pressione arteriosa diastolica. Anche in questo caso, non vi erano differenze tra pazienti più giovani e pazienti più anziani nell’efficacia di riduzione della pressione arteriosa con Barnidipina. La diminuzione della pressione media del polso dopo circa 3 mesi di terapia è stata maggiore nei pazienti > 55 anni (-10,8 mmHg) rispetto ai pazienti ≤ 55 anni (-8,7 mmHg), tendenza già visibile alla visita 2 (-8,2 mmHg e -6,5 mmHg, rispettivamente). La diminuzione della pressione media del polso è stata maggiore nei pazienti > 55 anni (-10,8 mmHg) rispetto ai pazienti ≤ 55 anni (-8,7 mmHg) e la percentuale di pazienti con pressione del polso > 60 mmHg è diminuita dal 61,1% al basale al 24,8% alla visita 3 nei pazienti >55 anni, e dal 47,7% al 16,5% nei pazienti ≤ 55 anni. Per quanto riguarda l’incidenza complessiva degli eventi avversi, questa è risultata essere bassa e ha portato all’interruzione del trattamento solo nel 3,0%-3,6% dei pazienti. L’edema periferico, un effetto avverso comune dei calcio-antagonisti nella pratica clinica, è stato riportato dal 2,7% dei pazienti di età < 65 anni e dal 4,6% dei pazienti di età ≥ 65 anni. Questi risultati supportano quindi sia l’efficacia sia la tollerabilità di Barnidipina nei pazienti più anziani come nei pazienti più giovani.
- Barnidipina può esercitare un effetto favorevole sulla disfunzione endoteliale nei pazienti ipertesi: risultati di uno studio preliminare (28)
Numerose evidenze dimostrano che l’ipertensione essenziale sia causa di disfunzione endoteliale, caratterizzata da fattori quali lo squilibrio tra vasodilatazione e vasocostrizione e l’aumento dello stress ossidativo che, a loro volta, contribuiscono al danno vascolare, allo sviluppo e alla progressione dell’aterosclerosi e all’insorgenza di eventi cardiovascolari (e.g. 29). Sulla base di questa premessa, uno studio italiano ha indagato gli effetti del trattamento antipertensivo (fino a 24 settimane) con Barnidipina rispetto a un diuretico tiazidico, l’idroclorotiazide, sulla funzione endoteliale in pazienti con ipertensione essenziale da lieve a moderata − pressione arteriosa diastolica da seduti di 90-109 mmHg e/o pressione arteriosa sistolica di 140-179 mmHg. Lo studio era randomizzato a gruppi paralleli, open-label. Dopo 2 settimane di run-in senza trattamento, i pazienti sono stati randomizzati per ricevere Barnidipina alla dose giornaliera iniziale di 10 mg, o idroclorotiazide alla dose iniziale giornaliera di 12,5 mg. Dopo 6 settimane di trattamento, nei pazienti non responsivi al trattamento il dosaggio giornaliero del farmaco è stato raddoppiato, mentre nei pazienti responsivi questo dosaggio è stato mantenuto fino alla fine dello studio (28). La funzione endoteliale è stata misurata attraverso la dilatazione flusso-mediata dell’arteria brachiale (FMD), una tecnica ecografica ad alta risoluzione non invasiva, ben tollerata e riproducibile. Dopo 12 e 24 settimane di trattamento, è stata osservata una riduzione significativa della pressione arteriosa clinica in entrambi i gruppi di trattamento. Inoltre, è stata osservata una riduzione significativa della pressione arteriosa sistolica e della pressione arteriosa diastolica nelle 24 ore nei pazienti che ricevevano Barnidipina, ma non in quelli che ricevevano il diuretico. Per quanto riguarda la funzione endoteliale, innanzitutto va notato che i valori del diametro al basale erano simili e non sono state osservate variazioni durante il trattamento in entrambi i gruppi di pazienti. Il valore medio della FMD misurato al basale, invece, era significativamente più alto nei pazienti sottoposti a terapia diuretica (6,88 ± 3,64% vs 3,9 ± 3,14%, p < 0,05 nei pazienti trattati con idroclorotiazide e Barnidipina, rispettivamente). Dopo 12 settimane di trattamento è stato osservato un significativo aumento della FMD nel gruppo Barnidipina, mentre una lieve riduzione, anche se non statisticamente significativa, della FMD endotelio-dipendente è stata trovata nel gruppo idroclorotiazide. Dopo 24 settimane di trattamento, un ulteriore lieve aumento della dilatazione endotelio-dipendente (anche se non statisticamente significativo rispetto al basale) è stato osservato nel gruppo Barnidipina. La riduzione della FMD osservata nel gruppo idroclorotiazide dopo 12 settimane è stata confermata a 24 settimane di trattamento (Figura 3). La variazione percentuale della FMD era diversa tra i pazienti trattati con Barnidipina (a 12 settimane 1,2 ± 2,2%, p < 0,023 e a 24 settimane 1,25 ± 3,15%, p < 0,16 dal basale) e quelli trattati con idroclorotiazide (a 12 settimane 1,0 ± 3,0%, p < 0,089 e a 24 settimane 1,78 ± 2,9%, p < 0,015 dal basale) (Figura 3). Considerando i valori di FMD prima del trattamento e alla fine dello studio, si può notare un aumento significativo della FMD a 24 settimane durante il trattamento con Barnidipina ma non durante la somministrazione di idroclorotiazide. Nell’intero gruppo, non è stata osservata alcuna correlazione significativa tra le variazioni della FMD e le variazioni della pressione arteriosa sistolica clinica. Al contrario, le variazioni della FMD a 6 mesi erano significativamente correlate alle variazioni del colesterolo LDL e del potassio sierico (28). Questi risultati suggeriscono quindi che, attraverso il trattamento con Barnidipina, ma non con un diuretico, è possibile ottenere un miglioramento della disfunzione endoteliale, valutata mediante ecografia non invasiva della dilatazione dell’arteria brachiale in risposta all’iperemia reattiva. Sebbene questo studio debba considerarsi pilota, a causa del numero ridotto di pazienti studiati, apre nuove prospettive per lo studio di ulteriori benefici di Barnidipina e degli altri calcio-antagonisti (28).
- Miglioramento dei parametri ecocardiografici in seguito a trattamento con Barnidipina in associazione a un sartano (30)
L’ipertrofia ventricolare sinistra (LVH), un marker di danno end-organ cardiaco, si riscontra frequentemente nei pazienti ipertesi ed è altamente predittiva delle complicanze cardiovascolari. Il diabete mellito è uno stimolo indipendente per l’LVH, che a sua volta può contribuire agli eventi cardiovascolari nei soggetti diabetici (31). Quando l’ipertensione è associata al diabete, lo sviluppo di LVH è ulteriormente accelerato e il rischio di complicanze cardiovascolari è quindi notevolmente aumentato. A oggi, il miglior trattamento della LVH è la sua identificazione precoce e la rapida implementazione di un trattamento adeguato: i bloccanti del recettore dell’angiotensina II (ARBs o sartani) e gli inibitori dell’enzima di conversione dell’angiotensina (ACE-inibitori) dovrebbero essere la terapia di prima linea, poiché si sono dimostrati i più efficaci nel ridurre l’LVH nei pazienti diabetici di tipo 2. Nei casi in cui gli ACE-inibitori o gli ARBs siano controindicati o non tollerati, o quando non sono sufficienti per raggiungere un adeguato controllo della pressione arteriosa, si dovrebbe aggiungere un altro agente antipertensivo, e i calcio-antagonisti potrebbero essere un’opzione come terapia di seconda linea (32). Questo studio ha quindi valutato gli effetti di Lercanidipina, un altro calcio-antagonista, rispetto a Barnidipina, entrambi in aggiunta a Losartan, su alcuni parametri ecocardiografici, in pazienti ipertesi, diabetici di tipo 2, con LVH. In questo studio italiano, multicentrico, randomizzato, in doppio cieco e controllato sono stati inclusi pazienti adulti con ipertensione da lieve a moderata, con diabete mellito di tipo 2, con LVH, non ben controllati da Losartan, con colesterolo lipoproteico a bassa densità (LDL) < 160 mg/dL, ambulatoriali in sovrappeso. I pazienti sono stati randomizzati a Lercanidipina 20 mg/die o Barnidipina 20 mg/die, in aggiunta a Losartan 100 mg/die per 6 mesi (30). Degno di nota, nessun paziente ha interrotto lo studio a causa di eventi avversi. Entrambi i trattamenti hanno indotto una riduzione simile e significativa rispetto al basale della pressione arteriosa sistolica e della pressione arteriosa diastolica, senza differenze statisticamente significative tra i due gruppi. Per quanto riguarda i parametri metabolici, il colesterolo LDL è stato ridotto da Barnidipina + Losartan, sia rispetto al basale che rispetto a Lercanidipina + Losartan, e l’acido urico è stato ridotto in entrambi i gruppi rispetto al basale (quest’ultimo effetto probabilmente dovuto all’assunzione concomitante di Losartan). L’indice di massa ventricolare sinistra, utilizzato come misura dell’LVH, è stato ridotto da entrambi i trattamenti, ma in misura maggiore da Barnidipina + Losartan (Tabella 1). Anche lo spessore del setto interventricolare in diastole è stato ridotto da Barnidipina + Losartan sia rispetto al basale che rispetto a Lercanidipina + Losartan (Tabella 1). Per tutti gli altri parametri presi inconsiderazione (Tabella 1) − riduzione dello spessore della parete posteriore in diastole; aumento del rapporto tra la velocità di riempimento diastolico precoce di picco e della velocità di riempimento di picco della contrazione atriale; riduzione del tempo di rilassamento isovolumetrico; riduzione dell’indice di volume atriale sinistro −, solo Barnidipina + Losartan sono stati efficaci, sia rispetto al basale che contro Lercanidipina + Losartan (30). Questi risultati dimostrano quindi innanzitutto che Barnidipina ha migliorato il colesterolo LDL. Poiché il dosaggio degli agenti ipocolesterolemizzanti che assumevano i pazienti, in sovrappeso, è stato mantenuto stabile durante tutto lo studio, gli effetti sul profilo lipidico sembrano essere strettamente legati a Barnidipina. Importante, questo studio dimostra un effetto positivo di Barnidipina sui parametri ecocardiografici, più efficace di Lercanidipina, con miglioramento dell’indice di massa ventricolare sinistra, dello spessore del setto interventricolare in diastole, dello spessore della parete posteriore in diastole e del tempo di rilassamento isovolumetrico. Questa differenza rispetto a uno studio precedente (33) è probabilmente dovuta alla maggiore durata del presente studio, 6 mesi vs 3 mesi. Inoltre, questo effetto positivo sui parametri ecocardiografici non sembra essere correlato alla riduzione della pressione arteriosa, perché anche il trattamento con Lercanidipina ne ha migliorato il controllo. Gli autori concludono che Barnidipina abbia probabilmente un’efficacia protettiva degli organi finali più pronunciata legata alle caratteristiche intrinseche di questo composto.
Conclusioni
Barnidipina è un calcio-antagonista lipofilo diidropiridinico indicato nel trattamento dell’ipertensione essenziale da lieve a moderata. Il dosaggio di Barnidipina una volta al giorno, la sua buona tollerabilità e l’effetto antipertensivo duraturo e dose-dipendente contribuiscono a un’ottima aderenza dei pazienti. Barnidipina è caratterizzata da una lenta insorgenza d’azione e da un legame forte e duraturo con i canali del calcio di tipo L. L’efficacia e la tollerabilità di Barnidipina sono comprovatamente comparabili in pazienti più giovani e pazienti più anziani. Uno studio pilota, inoltre, suggerisce che Barnidipina possa avere un effetto benefico sulla disfunzione endoteliale. Infine, Barnidipina in associazione a un sartano migliora i parametri ecocardiografici indipendentemente dalla riduzione della pressione arteriosa.
Bibliografia
- Zhou B, Carrillo-Larco RM, Danaei G, Riley LM, Paciorek CJ, Stevens GA, et al. Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. The Lancet. 2021 Sep 11;398(10304):957–80.
- Tocci G, Battistoni A, Passerini J, Musumeci MB, Francia P, Ferrucci A, et al. Calcium channel blockers and hypertension. J Cardiovasc Pharmacol Ther. 2015 Mar;20(2):121–30.
- Lewington S, Clarke R, Qizilbash N, Peto R, Collins R, Prospective Studies Collaboration. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet. 2002 Dec 14;360(9349):1903–13.
- More than 700 million people with untreated hypertension [Internet]. World Health Organization (WHO); 2021. Available from: https://www.who.int/news/item/25-08-2021-more-than-700-million-people-with-untreated-hypertension
- Volpe M. Calcium Channel Blockers for the Clinical Management of Hypertension. High Blood Press Cardiovasc Prev. 2018 Mar;25(1):1–3.
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. J Hypertens. 2018 Oct;36(10):1953–2041.
- Godfraind T. Discovery and Development of Calcium Channel Blockers. Frontiers in Pharmacology [Internet]. 2017 [cited 2022 Sep 23];8. Available from: https://www.frontiersin.org/articles/10.3389/fphar.2017.00286
- Elliott WJ, Ram CVS. Calcium channel blockers. J Clin Hypertens (Greenwich). 2011 Sep;13(9):687–9.
- Ambrosioni E, Borghi C. Calcium channel antagonists in hypertension. Am J Hypertens. 1989 Feb;2(2 Pt 2):90S-93S.
- Yokoyama S, Kaburagi T. Clinical effects of intravenous nifedipine on renal function. J Cardiovasc Pharmacol. 1983 Feb;5(1):67–71.
- van Zwieten PA, van Meel JC, Timmermans PB. Pharmacology of calcium entry blockers: interaction with vascular alpha-adrenoceptors. Hypertension. 1983;5(4 Pt 2):II8-17.
- Pasanisi F, Elliott HL, Meredith PA, Sumner DJ, Reid JL. Effect of calcium channel blockers on adrenergic and nonadrenergic vascular responses in man. J Cardiovasc Pharmacol. 1985;7(6):1166–70.
- Staessen JA, Fagard R, Thijs L, Celis H, Arabidze GG, Birkenhäger WH, et al. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. The Systolic Hypertension in Europe (Syst-Eur) Trial Investigators. Lancet. 1997 Sep 13;350(9080):757–64.
- Liu L, Zhang Y, Liu G, Li W, Zhang X, Zanchetti A, et al. The Felodipine Event Reduction (FEVER) Study: a randomized long-term placebo-controlled trial in Chinese hypertensive patients. J Hypertens. 2005 Dec;23(12):2157–72.
- Dahlöf B, Hansson L, Lindholm LH, Scherstén B, Wester PO, Ekbom T, et al. STOP-Hypertension 2: a prospective intervention trial of “newer” versus “older” treatment alternatives in old patients with hypertension. Swedish Trial in Old Patients with Hypertension. Blood Press. 1993 Jun;2(2):136–41.
- Brown MJ, Palmer CR, Castaigne A, de Leeuw PW, Mancia G, Rosenthal T, et al. Morbidity and mortality in patients randomised to double-blind treatment with a long-acting calcium-channel blocker or diuretic in the International Nifedipine GITS study: Intervention as a Goal in Hypertension Treatment (INSIGHT). Lancet. 2000 Jul 29;356(9227):366–72.
- Malacco E, Mancia G, Rappelli A, Menotti A, Zuccaro MS, Coppini A, et al. Treatment of isolated systolic hypertension: the SHELL study results. Blood Press. 2003;12(3):160–7.
- Malhotra HS, Plosker GL. Barnidipine. Drugs. 2001;61(7):989-996. doi:0012-6667/01/0007-0989/$27.50/0
- Liau CS. Barnidipine: A new calcium channel blocker for hypertension treatment. Expert Rev Cardiovasc Ther. 2005;3(2):207-213. doi:10.1586/14779072.3.2.207
- Janssen BJA, Kam KL, Smits JFM. Preferential renal and mesenteric vasodilation induced by barnidipine and amlodipine in spontaneously hypertensive rats. Naunyn-Sclrn1iedeberg’s Arch Pharmacol. 2001;364:414-421. doi:l 0.1007 /s002 l 00 l 00468
- Teramura T, Watanabe T, Higuchi S, Hashimoto K. Metabolism and pharmacokinetics of barnidipine hydrochloride, a calcium channel blocker, in man following oral administration of its sustained release formulation. http://dx.doi.org/101080/004982597240695. 2008;27(2):203-216. doi:10.1080/004982597240695
- Wegener JW, Meyrer H, Rupp J, Nawrath H. Barnidipine block of L-type Ca2+ channel currents in rat ventricular cardiomyocytes. Br J Pharmacol. 2000;130(8):2015-2023. doi:10.1038/SJ.BJP.0703514
- Lins R, de Vries C. Efficacy and Tolerability of Barnidipine in Real-Life Arterial Hypertension: Results from Younger and Older Patients in the BASIC-BT Study. The Open Cardiovasculur Medicine Jourual. Published online 2017.
- Naber FB, Häge R, Mortelmans J. Barnidipine monotherapy and combination therapy in older patients with essential hypertension: a long-term study. Int J Clin Pract Suppl. 2000;114:27-35.
- Otterstad JE, Ruilope LM. Treatment of hypertension in the very old. Int J Clin Pract Suppl. 2000;114.
- Lins R, Marckx P, Vandebeek R, Vanhoutvinck C, Neuville O. Barnidipine real-life tolerability in arterial hypertension: results from the BASIC-HT study. http://dx.doi.org/101179/2295333715Y0000000012. 2015;70(4):244-250. doi:10.1179/2295333715Y.0000000012
- (UK) NCGC. Hypertension. NICE. Published online 2011. Accessed October 17, 2022. https://www.ncbi.nlm.nih.gov/books/NBK83274/
- Muiesan ML, Salvetti M, Belotti E, et al. Effects of barnidipine in comparison with hydrochlorothiazide on endothelial function, as assessed by flow mediated vasodilatation in hypertensive patients. Blood Press. 2011;20(4):244-251. doi:10.3109/08037051.2011.561072
- Muiesan ML, Salvetti M, Paini A, et al. Prognostic role of flow-mediated dilatation of the brachial artery in hypertensive patients. J Hypertens. 2008;26(8):1612-1618. doi:10.1097/HJH.0B013E328304B083
- Derosa G, Mugellini A, Querci F, et al. Barnidipine or Lercanidipine on Echocardiographic Parameters in Hypertensive, Type 2 Diabetics with Left Ventricular Hypertrophy: A Randomized Clinical Trial. Sci Rep. 2015;5. doi:10.1038/srep12603
- Nielsen FS et al. Left ventricular hypertrophy in non-insulin-dependent diabetic patients with and without diabetic nephropathy. Diabet Med. 1997;14:538-546.
- Derosa G, Maffioli P. Assessment and management of left ventricular hypertrophy in Type 2 diabetes patients with high blood pressure. http://dx.doi.org/101586/erc1336. 2014;11(6):719-728. doi:10.1586/ERC.13.36
- Angell F, Repaci S, Borgioni C, Sardone M, Scotti A, Verdecchia P. Effects of barnidipine on blood pressure and left ventricular diastolic function in patients with hypertension and metabolic syndrome: A 12-week, open-label noncomparison study. Current Therapeutic Research. 2008;69(3):207-220. doi:10.1016/J.CURTHERES.2008.06.003
Related papers
Lo scenario della medicina attuale è caratterizzato da elementi di complessità generale inimmaginabili due decenni fa ed in grado di rendere molto più difficile la pratica clinica giornaliera. In particolare, la coesistenza di multiple condizioni passibili di un trattamento farmacologico nello stesso soggetto condiziona in maniera forzata alcune delle scelte terapeutiche spingendo alla ricerca di [more info]
Premessa Nell’ultimo decennio l’orizzonte della terapia ipolipemizzante si è arricchita di formidabili strumenti terapeutici quali ezitimibe, inibitori della proteina PCSK9 (PCSK9i) e acido bempedoico. Gli studi su queste molecole hanno permesso non solo di dimostrarne l’efficacia, ma hanno fornito importanti informazioni sull’importanza dell’abbassamento delle LDL nella riduzione del rischio cardiovascolare (CV) e costituiscono la base [more info]
Colesterolemia subottimale come fattore di rischio per le malattie cardiovascolari Il miglioramento delle abitudini alimentari e l’ottimizzazione dei livelli di colesterolo LDL nel sangue – fattore causale e cumulativo - sembrano essere strumenti efficaci per ridurre il rischio di malattie cardiovascolari su base aterosclerotica, che ancora oggi rappresentano una delle principali cause di morte e [more info]